【フェムテック法務】郵送検査キット参入の適法ルート|アプリ化・SaMD化を見据えた戦略的選択肢
行政書士の大串です。国内のフェムテック・フェムケア市場は、一時の過熱状態は落ち着いたような肌感があるかもしれません。しかしあるレポートでは、2025年に約888億円規模にまで拡大すると見込まれているところですし[1]、そもそも人間の半分は女性ですからね。特に更年期ケアやプレコンセプションケアの市場についてはまだ伸びるだろうと予測しています。
この成長の背景には、経済産業省が試算した「女性特有の健康課題による年間約3.4兆円の経済損失」という深刻な課題に対し、企業の福利厚生やD2Cサービスが解決策を提示し始めたことがあります[2]。
この成長市場において、多くの事業者が検討するビジネスのひとつとして、「郵送検査サービス」があります。近年はAIを冠したものも目につくようになってきましたね。しかし、このビジネスモデルは薬機法、医師法、臨床検査技師法などが複雑に交差する領域でのビジネスですから、思いつきで手を出すと大火傷。令和8年3月31日に発出された最新ガイドライン[4]をはじめ、適法な着地点を見出すための規制理解が不可欠な分野です。そして実務上さらに重要なのは、法律の条文を満たすことの先にある「事業としての倫理観」です。
本記事では、将来的な「アプリ連携」や「SaMD(プログラム医療機器)化」までを視野に入れつつ、事業者が今選ぶべき3つの適法ルートについて提示申し上げます。
まず大前提として、本記事で扱うのは、ユーザーが採取した検体を衛生検査所へ送り、後日結果を閲覧する「受託検査モデル(検体検査モデル)」です。

「検体検査」の法的な定義については、こちらの記事で詳しく解説しています。[関連記事:検体検査の法的定義とは?薬機法・臨床検査技師法上の整理]
なお、その場で判定結果が出る「体外診断用医薬品(IVD)」は、それ自体で検査が完結し、「郵送検査サービス」の枠組みに該当しなくなるため、本稿の検討対象からは除外します。これに加えて、「明らかに研究機関等のみを対象としたキット」もまた、郵送検査サービスの枠組みに該当しないため、本稿の検討対象からは除外します。

その場判定型の「体外診断用医薬品(IVD)」については、以下の記事をご参照ください。[関連記事:自宅で完結!セルフ検査キット(体外診断用医薬品)の基礎知識]
現行の薬機法規制および最新のガイドライン[4][5]を踏まえ、現実的な3つのルートを定義しました。
そもそも「郵送検査サービス」とは何か:既存の医療検査との対比
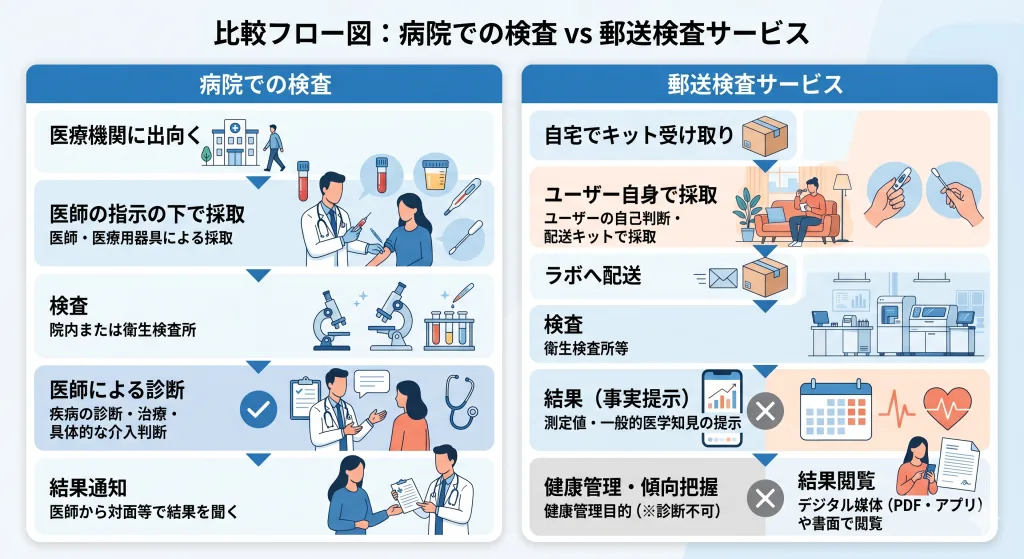
病院で行われる検査の「採取工程」をユーザー自身の手に委ねるのがこのビジネスの核心です。
| 比較項目 | 従来の病院・診療所での検査 | 郵送検査サービス |
|---|---|---|
| ① どこで(場所) | 医療機関に出向いて実施 | 自宅や外出先など、任意の場所 |
| ② 何を(検体・指標) | 尿、血液、組織、心拍・呼気・身長体重などの生体指標 | 尿、血液(自己採血・経血)、唾液、便、膣分泌液等 |
| ③ 誰が・何で(採取) | 医師の指示の下、医療用器具で採取 | ユーザーの自己判断で、ユーザー自身が配送されたキットで採取 |
| ④ 誰から(結果) | 後日、医師から対面等で結果を聞く | デジタル媒体(PDF・アプリ等)や後日送付される書面で閲覧 |
| ⑤ なんのために(目的) | 疾病の診断・治療や、具体的な介入判断 | 健康管理・傾向把握(※診断目的は不可) |
| ⑥ 検査機能の所在 | 医療機関または衛生検査所 | 衛生検査所、またはその他の機関 |

採取された検体を「誰が検査できるのか」という主体についての法規制は、こちらの記事で網羅しています。[関連記事:人から採取した検体は誰が検査できる?衛生検査所の登録と注意点]
なぜ「フェムテック」において郵送検査が重要なのか
郵送検査市場の中でも、特にフェムテック領域で導入が加速している理由は、女性特有の受診構造と最新の採取テクノロジーにあります。
- 心理的・物理的ハードルの解消:子宮頸がん(HPV)や膣内フローラ等の検査において、内診台への抵抗感から受診を控えるケースは少なくありません[3]。
- 非侵襲的な採取技術の進化:従来の指先穿刺(ランセット)による自己採血に加え、近年では「経血」を検体として活用する技術(ユニ・チャームや株式会社asaiなどの取り組み)が注目されています。ナプキン型デバイス等による非侵襲的な採取は、ユーザーの負担を最小化し、「検査」を日常のケアの延長線上に位置づけました。
- ライフステージによる周期的な需要:月経、妊活、更年期といった変化に伴い、ホルモンバランスや生体指標を「定点観測」したいというニーズに合致しています。
自社の関わり方はどれ?3つの適法ルート比較表
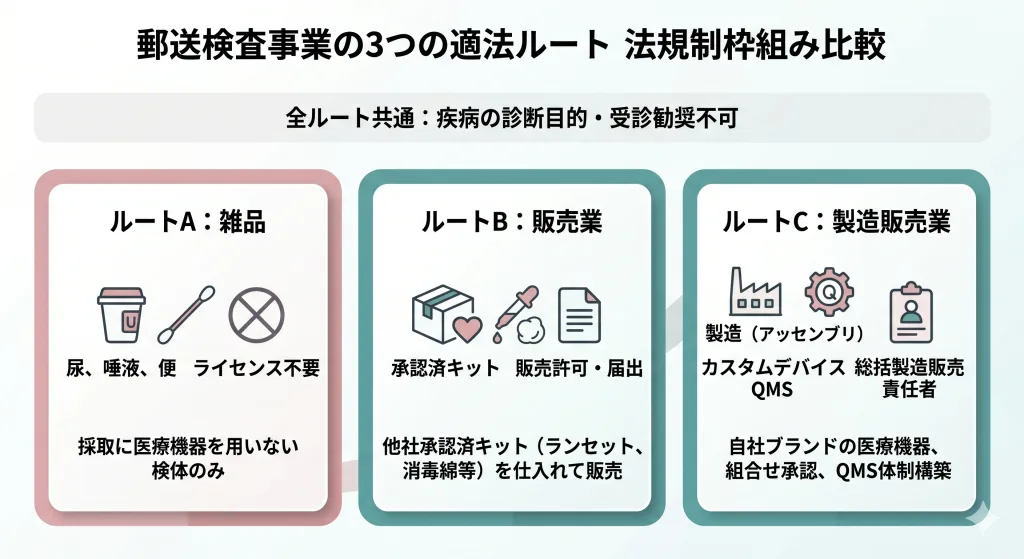
現行の薬機法下では、検体を検査して「疾患リスクの提示」や「受診勧奨」を行うものは、疾病の診断目的として規制対象となります。どのルートを選んでも、結果通知において受診勧奨を行うことや具体的な疾患を想定させる表現はできないという厳しい現実に留意が必要です。
また、ルートB・Cにおいて「自己採血セット」を扱う場合、自己採血に必要な「消毒用綿(医薬品たる外皮用殺菌消毒剤)」と医療機器(ランセット等)を一組にして販売することが実務上の標準となっています。これらはコンビネーション製品ではなく「組合せ医療機器」として取り扱われる点に留意が必要です[6]。
| 評価項目 | ルートA:医療機器なし(雑品) | ルートB:既製品活用(販売業) | ルートC:自社セット組(製販) |
|---|---|---|---|
| 採取器具 | 雑品(採尿コップ、綿棒等) | 他社承認済みの組合せ医療機器(ランセット・消毒綿等)同梱キット(そのまま販売) | 組合せ医療機器(自社承認/アッセンブリ) |
| 検体 | 唾液、尿、便など(採取に医療機器を用いないもの) | 尿、血液(経血含む)、その他(採取に医療機器を用いるものを含む) | 尿、血液(経血含む)、その他(採取に医療機器を用いるものを含む) |
| 必要な許可 | 特になし | セットに含まれる医療機器のクラスに応じた販売業の許可又は届出が必要(※1) | 医療機器製造販売業/製造業(※2) |
| 製品の法的性格 | 雑品(検査資材) | 既承認の組合せ医療機器 | 自社ブランドの医療機器/組合せ承認 |
| 結果の提示 | 一般的医学知見の提示のみ | 測定値・一般的医学知見の提示 | 測定値・一般的医学知見の提示 |
| 最大の障壁 | 診断・受診勧奨の禁止 | 広告表現・説明図の制限 | QMS体制構築、承認取得コスト |
※ルートBについては、製造販売業者が販売している「自己採血セット(組合せ医療機器)」を仕入れて販売するスキームを想定しています。(※1)組合せ医療機器として承認されていれば、医療機器販売業のライセンスで流通可能[6]。(※2)組合せ医療機器として自社承認を得る場合、製造販売業として薬事責任を負う[6]。
ルートA:医療機器を使わないルート(非侵襲・雑品)
尿や唾液など、人体を傷つけない検体のみを扱うモデルです。
- 構築のポイント: 採取器具が「雑品」に該当するため、最も低コストで参入可能です。
- 法的制約: 「診断には使えません」と書いてあっても、販売ページで特定の疾患名を挙げて「安心のために」等と標榜すれば、即座に無承認の疾病診断目的(IVD/医療機器)とみなされます。結果通知においても、「陽性」「異常」といった判定や「医療機関へ」という勧奨はできません。
ルートB:医療機器の既製品を扱うルート(販売業)
他社が既に「組合せ医療機器」等として承認を得ている自己採血キットを仕入れ、サービスと組み合わせて販売するモデルです。
- 組合せ医療機器としての性質: 自己採血に必要なランセット(穿刺する医療機器)と、穿刺部位を消毒するためのアルコール綿(医薬品たる外皮用殺菌消毒剤)を組み合わせて包装・滅菌したものは、薬機法上「組合せ医療機器」に該当します[6]。事業者はこれを医療機器として仕入れ、適切な医療機器販売業の届出・許可の下でキットを流通させることが可能になります。
- 必要なライセンス: セットに含まれる医療機器のクラス(高度管理医療機器、管理医療機器など)に応じた、販売業の許可又は届出が必要です。一般的に自己採血に用いるランセットなどは管理医療機器に該当することが多いため、管理医療機器販売業の届出が中心となります。
- 構築のポイント: 自社でアッセンブリ(セット組)を行うと上述の「製造」に該当してしまうため、他社承認済みの組合せ医療機器パッケージをそのまま扱う必要があります。
- 採取の説明: 独自に人から検体を採取するための図示や説明を詳細に行うことは、診断目的を暗示するものとして現行法下で厳しく制限されます。添付文書の範囲内での説明に留める実務が必要です。
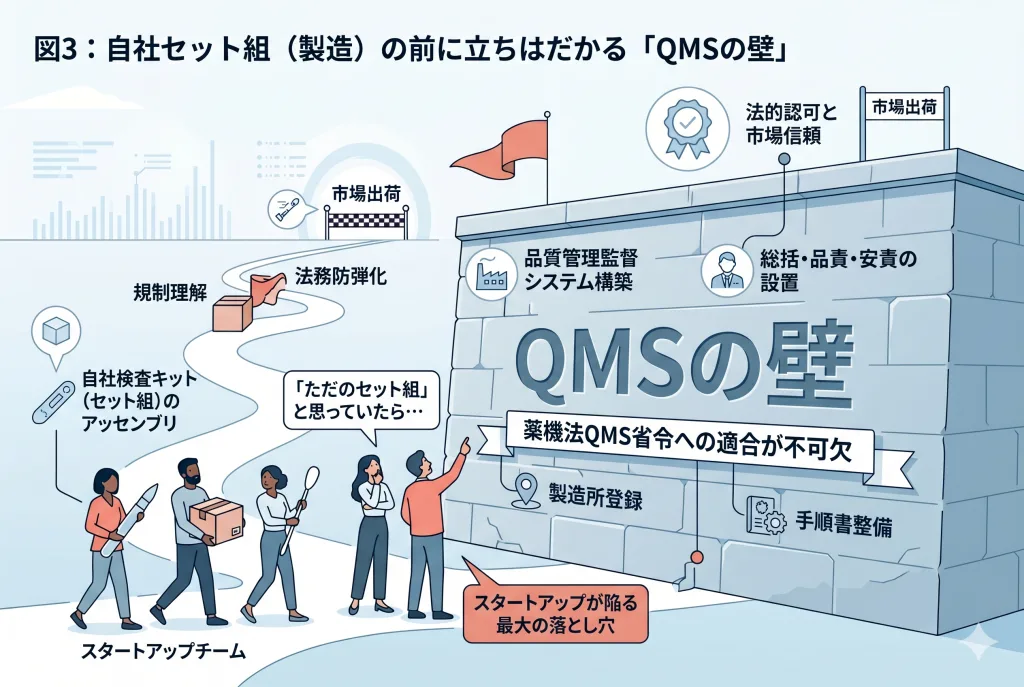
ルートC:自社で責任を負う本格ルート(製造販売業/製造業)
自社ブランドとして採取キットを企画し、医療機器として市場に送り出すモデルです。
- 必要なライセンス:
- 医療機器製造販売業: 総括製造販売責任者を置き、QMS体制を構築して製品に責任を持つ。医療機器としての承認・認証の枠組みの中で、セットされる医薬品(アルコール綿等)についても品質管理責任を負うことになります[6]。
- 医療機器製造業: 実際にアッセンブリ(セット組)を行う施設に必要。
- 構築のポイント: 組合せ医療機器としての承認、または既存製品のOEM供給を受け自社名で販売します。
- 実務上の注意: 前述のQMS体制の維持コストが最も重くのしかかるルートですが、将来的なアプリの医療機器化(SaMD)を見据える場合、この体制構築は不可避です。

ルートCへの本格参入を目指す場合、薬事三役の確保が最大の壁となります。
「データの示し方」の進化:アプリ活用の展望と法的リスク
郵送検査ビジネスにおける顧客体験は、今や「報告書を受け取る」ことから、「アプリで自分の健康状態をマネジメントする」ことへと劇的に変化しています。
かつて主流だったPDF形式のレポート返却は、単発の数値報告に過ぎませんでした。しかし現在では、スマートフォンアプリを活用することで、検査結果の時系列での可視化(トレンド分析)や、基礎体温・歩数・睡眠時間といったウェアラブルデバイス由来のデータとの統合が可能になっています。
「診断行為」のグレーゾーン:何を伝え、何を伝えないか

データの見せ方が高度になればなるほど、ソフトウェアとしての法規制(SaMD該当性)が牙を剥きます。ここで重要になるのは、「疾病の診断」と「健康管理の支援」の境界線です。
- OK例(健康管理支援): 「貴方の数値は●●です。これは一般的な参照値(〇〇〜△△)を上回っています」「過去3回の平均値と比較して〇%の上昇傾向にあります」といった、医学的知見に基づいた客観的な事実の提示や、日常的な健康管理の目安としての情報提供に留める構成。
- NG例(疾病の診断): 「検査結果に基づき、●●病の疑いがあります」「あなたは不妊症の可能性が高いです」といった断定的な表現。これらは医師のみが許される「診断」に該当し、アプリはSaMDの承認が必要となります。

アプリが「プログラム医療機器(SaMD)」に該当させるのか、させないのか。その意図にあわせた設計が重要です。具体的な境界線については、以下の記事で詳しく解説しております。
単なるグラフ表示を超えて、AIが特定の疾患リスクを自動判定してユーザーに突きつけたり、具体的な治療方針を示唆したりする設計は、プログラム医療機器(SaMD)に該当し、疾病の診断目的を有するものとして現行法下で厳格に管理されるべき領域となります。
結論:新ガイドライン下での生き残り戦略
令和8年3月31日の新ガイドライン[4]はキット自体に検査機能を持つ製品を対象としていますが、郵送検査においても現行の薬機法に基づき「疾患の罹患リスク提示」や「受診勧奨」は厳しく規制されています。
郵送検査サービスが適法に存続するためには:
- 採取器具の法的ステータス(雑品か、組合せ医療機器としての販売業か製販業か)を明確にする。
- QMS体制構築のコストを正しく見積もり、安易な「セット組」での自社ブランド化を避ける。
- SaMDでないならば、アプリでのフィードバックから「診断」を徹底的に排除し、あくまでユーザーの「客観的な自己理解を助ける事実提示」としての設計を貫く。
これらを遵守した上で、アプリ等を通じて「一般的な健康のヒント」を提供し、ユーザーのセルフケアを支援するモデルを構築することが、現在の最適解といえます。

「そのビジネスモデル、行政相談の前に『法務の防弾化』は済んでいますか?」
郵送検査とアプリを組み合わせたフェムテック事業は、令和8年の新ガイドライン施行により、これまで以上に「意図せぬ未承認医療機器の販売」や「無資格者による診断行為」と見なされるリスクが高まっています。
行政(薬務課・保健所)への事前相談は重要ですが、「何を、どう話すか」のロジックが固まっていない状態での相談は、かえって事業の首を絞めることになりかねません。
当事務所では、以下のような実務コンサルティングを提供しています。
- 貴社ビジネスモデルの「薬機法・医師法・臨床検査技師法」適合性
- アプリUI/UXにおける「非SaMD・非診断行為」を維持するための表現へのアドバイス
- 組合せ医療機器としての導入戦略とライセンス設計のサポート
「この表現はセーフか?」「このスキームで許可が通るか?」といった具体的な不安をお持ちの方は、まずは下記お問い合わせフォームよりご相談ください。貴社のイノベーションを、確かな法務戦略で形にします。
参考(参考文献・関連URL)
- 矢野経済研究所.“フェムケア&フェムテック(消費財・サービス)市場に関する調査を実施(2025年)”.矢野経済研究所.2025-10-23.https://www.yano.co.jp/press/press.php/003950,(参照 2026-04-28).
- 経済産業省.“女性特有の健康課題による経済損失の試算結果を公表しました”.経済産業省.2024-02-09.https://www.meti.go.jp/policy/mono_info_service/healthcare/downloadfiles/jyosei_keizaisonshitsu.pdf,(参照 2026-05-07).
- Teal Health.“US Clinical Study Demonstrates At-Home Screening is as Accurate as In-Clinic and Preferred by 94% of Women”.Teal Health.2025-05-09.https://www.getteal.com/research/u-s-clinical-study-demonstrates-94-of-women-prefer-at-home-cervical-cancer-screening,(参照 2026-05-07).
- 厚生労働省.“研究用と称する検査キット等の体外診断用医薬品の範囲に関するガイドラインについて(医薬監麻発0331第1号)”.2026-03-31.https://www.mhlw.go.jp/hourei/doc/tsuchi/T260401I0080.pdf,(参照 2026-05-07).
- 厚生労働省.“研究用と称する検査キット等の体外診断用医薬品の範囲に関するガイドライン(案)に関する意見募集の結果について”.2026-03-31.https://public-comment.e-gov.go.jp/pcm/download?seqNo=0000311330,(参照 2026-05-07).
- 厚生労働省.“「コンビネーション製品の承認申請における取扱いについて」の改正等について(薬生機発0628第1号)”.2019-06-28.https://www.mhlw.go.jp/web/t_doc?dataId=00tc2324&dataType=1&pageNo=1,(参照 2026-05-07).
免責事項
本記事の内容は、公開日時点の法令・ガイドラインに基づき作成しております。個別の事案については、行政の判断はご状況に応じ変わってまいりますので、必ず専門家や管轄の行政にご相談ください。
お気軽にご相談ください。
- 初回相談は無料です。
- 行政書士には秘密保持の義務が課せられております。
- フォームに入力されたメールアドレス以外に、当事務所から連絡差し上げることはいたしません。