【2026年最新】ヘルスケアアプリはどこから「医療機器プログラム(SaMD)」? 該当性基準とビジネスモデルの分岐点
行政書士の大串です。スマートフォンやスマートウォッチなど、身近なデバイスを活用したヘルスケアアプリケーションの開発が広がりを見せてますね。ライフログが大好きないち消費者として大歓迎のこの流れ。でも開発側の方たちにとってはヘルスケア・ウェルネスのアプリ開発領域は、意外と技術面以外で時間を取られることが多い、ということも存じ上げております。
ここで質問です。開発をしているときに、「私たちのアプリって、医療機器(SaMD)になるの?ならないの?」という疑問が、ふと頭をよぎったことはないでしょうか?はたまた、資金調達の相談に行ったときや、販売店やクラウドファンディングのプラットフォームさんに打診したときに尋ねられて答えに窮したことは?
この「医療機器への該当・非該当」の線引きですが、見誤ると、後になって取り返しのつかない手戻りが発生する可能性がある問いです。後になって判明して手戻りだなんてせっかくの技術の無駄遣い!ぜひ開発初期に線引きを理解し、方針を定めて邁進していただきたいという思いからこの記事を書いております。
というわけで、この記事では、医療機器プログラム(SaMD)の該当性について、さくっと解説して参ります。
【結論】医療機器プログラム(SaMD)の定義と判断のポイント
まずは、開発者が最初に押さえておくべき「該当性」の全体像を整理しましょう。
医療機器界隈において、健康に関与するアプリケーションは、2つに分類することができます。「医療機器プログラム」か「それ以外(雑品)」か、です。
前者の「医療機器プログラム」は、SaMD(サムディー、Software as a Medical Device)とも称されます。というか、医療機器界隈の方たちもSaMD呼びの方は多いですね。私もそうです。蛇足として私がSaMDと呼ぶ理由を書かせていただくと、医療機器界隈では「医療機器プログラム」と「プログラム医療機器」とは別のものを指すけれど、どっちどっちかわからなくなりがちだから、です。

「医療機器プログラム」と「プログラム医療機器」の違いを知りたい人向けのミニ説明。考えれば考えるほど混乱してくる気がしませんか…?
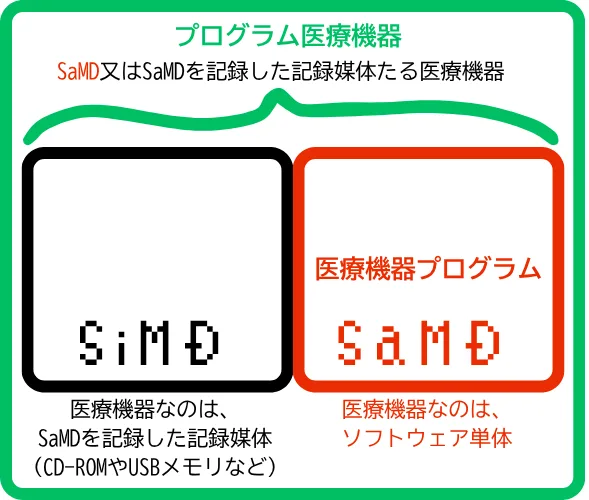
① 医療機器プログラム = SaMDの本質
解説は下に示します。ソフトウェア単体で医療機器としての機能を持つものを指します。
② プログラム医療機器 = SaMD又はSaMDを記録した”モノ”
薬事法施行規則第1条第3項では、「医療機器プログラム又はこれを記録した記録媒体たる医療機器」と定義されています。 つまりプログラム医療機器=「SaMD又はSiMD(Software in a Medical Device)」ということです。
③SiMD =「医療機器プログラム」をCD-ROMやUSBメモリなどに記録した、”モノ”としての医療機器を指す言葉です。
1. 医療機器プログラム(SaMD)とは?
さて、話を戻します。
医療機器プログラムとは、ですが、これが薬機法上にスパッと定義がないんですよね。ですので厚労省の資料から引っ張ってきたものを整理すると以下のようになります。
医療機器プログラムとは [1]
- 医療機器プログラムとは、医療機器の定義に該当する使用目的を有しているプログラムであって、
- それをインストール等することによってデスクトップパソコン等の汎用コンピュータ又はスマートフォン等の携帯情報端末(以下「汎用コンピュータ等」という。)に医療機器としての機能を与えるもの、
- あるいは既存の医療機器にインストール等することで医療機器たる更なる機能を付与するもの
- ただし、副作用又は機能の障害が生じた場合においても、人の生命及び健康に影響を与えるおそれがほとんどないものを除く
医療機器の定義(薬機法第2条第4項):この法律で「医療機器」とは、人若しくは動物の疾病の診断、治療若しくは予防に使用されること、又は人若しくは動物の身体の構造若しくは機能に影響を及ぼすことが目的とされている機械器具等(再生医療等製品を除く。)であつて、政令で定めるものをいう。
さて、これで医療機器プログラムとは何かが固まりましたね。では続いて、これに該当するか否かを行政がどう判断しているのか、を知っていきましょう。
2. 医療機器プログラムに該当するかどうかの判断基準
製品の表示、説明資料、広告などから判断されます。ポイントは以下の2つの要素です。
- 使用目的: そのプログラムが医療機器の定義に該当する使用目的を有しているか。
- リスクの程度: プログラムが誤作動した場合に、人の生命や健康に影響を与えるおそれがあるか(概ねクラスII以上のリスクがあるか)。
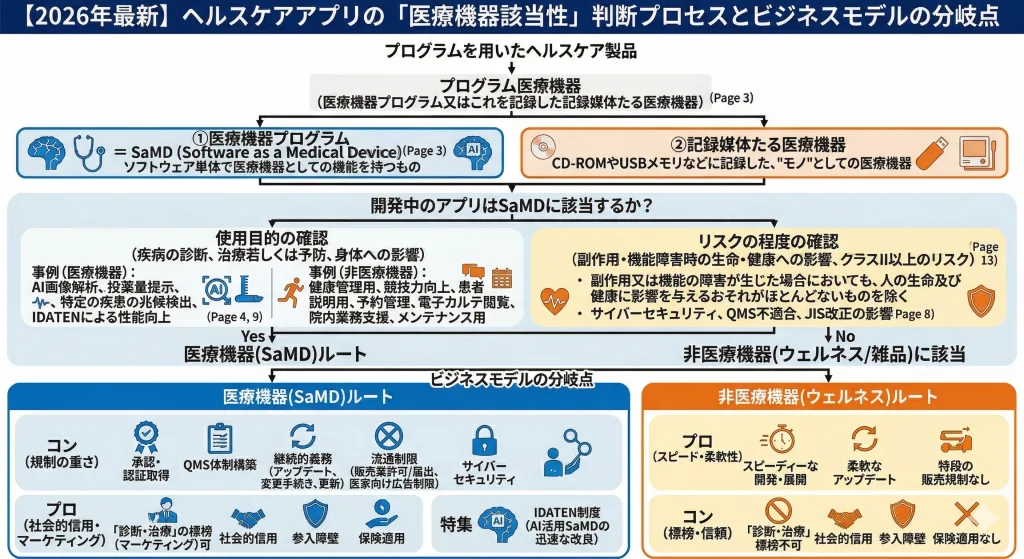
3. 【事例】SaMDに「該当するもの」と「該当しないもの」
具体的にどのようなアプリが該当するのかしないのか、典型的な例を挙げます[1][2]。
| カテゴリー | 該当する(医療機器)例 | 該当しない(非医療機器)例 |
|---|---|---|
| データ解析 | ▷AIが画像を解析し、がんの疑い部位を特定して医師に提示するためのプログラム | ▷体重や血圧の数値を記録し、単にグラフ化して表示するための、個人の健康・運動管理用プログラム ▷競技力向上や体力向上等のためのスポーツトレーニング管理プログラム(病態の把握や診断の兆候検出を目的としないもの) |
| 治療・介入 | ▷アルゴリズムに基づき、患者ごとに最適な投薬量や治療方針を提示するためのプログラム | ▷医療関係者が患者や家族に治療方法などを説明・理解してもらうための患者説明用プログラム ▷一般的なストレッチや食事メニューを、健康維持のために提案するためのプログラム |
| 受診勧奨 | ▷特定の疾患の兆候を検出し、「心房細動の疑い」等として受診を促すためのプログラム | ▷病院の予約管理や、電子カルテの単なる閲覧システムためのプログラム |
| 院内業務支援・メンテナンス | ▷医療関係者が患者の過去の診療記録の閲覧、健康記録等を記録・閲覧・転送するプログラム ▷診療予約や受付・会計業務の負担軽減等を目的とした院内業務支援プログラム ▷医療機関に医療機器の保守点検や消耗品の交換の時期等を伝達するメンテナンス用プログラム |
同じ「データを転送・分析する」機能を持つプログラムであっても、「疾病の診断や治療」を目的としていれば医療機器に該当する可能性が高く、単なる「日常の健康管理」が目的であれば該当しない可能性が高くなります。このあたりは明確な線引があるわけではなく、個別具体的な検討が必要です。
ビジネスへの影響(プロコン比較)
医療機器として進むか、ウェルネス機器として進むかで、その後のビジネスモデルは大きく変わります。
| 項目 | 医療機器(SaMD)に該当する場合 | 非医療機器(ウェルネス機器)の場合 |
|---|---|---|
| 規制・承認・認証・市販後の対応 | 薬機法に基づく厳格な規制(QMS体制構築、業許可・業登録、認証・承認の取得、臨床・非臨床評価など)が必要 【継続的義務とハードル】がある ①5年ごとに業許可等の更新、QMS適合性調査が必要②ライフサイクル全体で「医療機器基本要件基準」に適合し続ける義務(JIS規格改正や新たなセキュリティリスク出現等への随時対応)③製品変更時は、原則として事前・事後の薬事手続きが必要 | 薬機法の承認・認証プロセスが不要で、スピーディーな開発・展開が可能 頻繁なアップデートや仕様変更も、薬機法上の複雑な手続きを経ることなく柔軟・迅速に行える |
| 流通・販売 | 販売業の許可や届出等が必要となり、流通ルートに制限が生じる | 特段の薬機法上の販売規制はなく、一般市場へ直接提供可能 |
| 広告・標榜 | 「診断・治療」等の承認・認証を受けた医学的効果の標榜が可能(※ただし医家向けの場合、一般向け広告には制限あり)[4] | 「診断・治療」といった効果を広告等で標榜することは一切不可 |
どちらに傾けるかは「事業判断」。プロコンは意外と釣り合っている
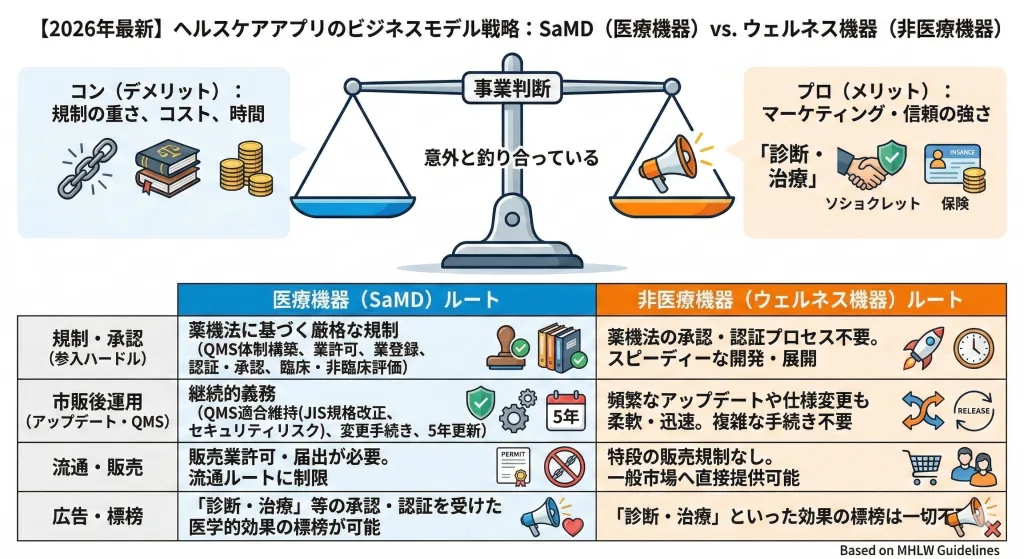
上記の比較表を見ると、医療機器に該当させることはデメリットばかりのように感じられるかもしれません。しかし、実際は多くのスタートアップが依然として医療機器化(SaMD化)を目指していらっしゃいます。それには、それを補って余りある理由があるからでしょう。
- 「標榜(マーケティング)」の圧倒的なパワー: ウェルネス機器では、どれほど優れたアルゴリズムであっても「〇〇病の診断を支援します」「〇〇を治療します」と広告で謳うことは一切できません。一方、医療機器として承認を得れば、承認・認証を受けた範囲で堂々と標榜でき、ユーザーや医療機関に対する訴求力は劇的に高まります。
- 参入障壁と社会的信用: 薬機法の高い壁は、乗り越えた瞬間からビジネスを保護する盾となります。またそれを乗り越えたという事実は、投資家からの資金調達や医療機関への導入において絶大な信頼の証となります。
つまり、このプロコンは「規制の重さ」と「マーケティング・信頼の強さ」で意外にも均衡しています。スピードを優先して一般市場で広く戦うか、コストと時間をかけてでも医療現場の「本丸」を狙うか。これは法的な該非判定であると同時に、極めて重要な「事業判断」の分岐点なのです。だから冒頭で申し上げた通り、開発初期に線引きを理解し、どちらに向けて開発するかの方針を定めていただきたいのです。
改めて。医療機器の該当性がビジネスを左右する理由
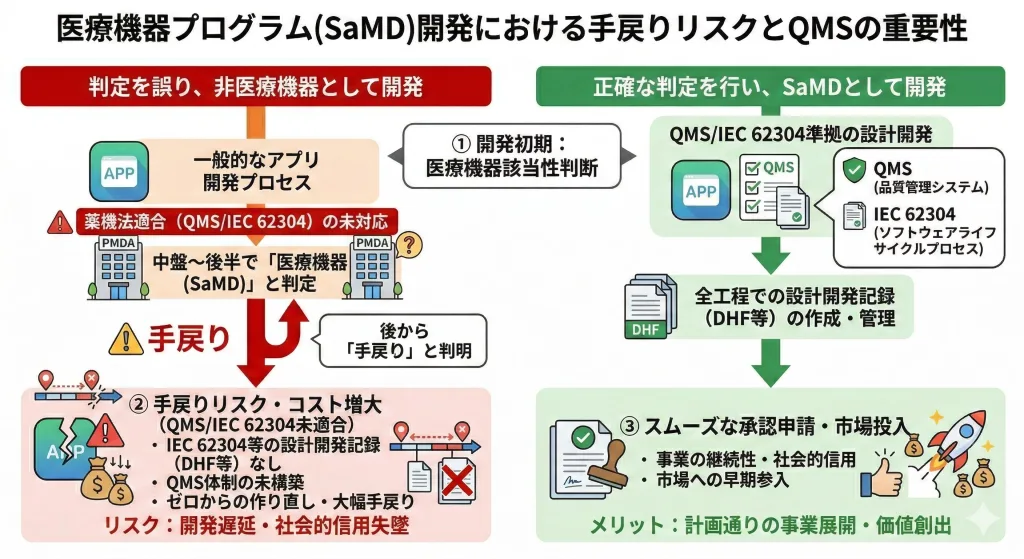
さてここで冒頭で申し上げていたことを、改めてお伝えします。
スタートアップの皆様が「素晴らしいアルゴリズムができた。あとはアプリにしてリリースするだけだ!」と意気込まれるお気持ちはよく分かります。しかし、法務・薬事の観点から見ると、ここに思わぬ落とし穴が潜んでいることがあります。
実務の現場であるある、かつ非常に困るのが、「自分たちは単なる健康管理アプリ(非医療機器)を作るつもりだったのに、いざPMDA(医薬品医療機器総合機構)や行政に相談したら『医療機器に該当する』と判定されてしまった」というケースです。医療機器に該当することが後から判明すると、非医療機器にすることにしても大幅な手直しが発生しますし、医療機器として進むことを選択しても医療機器開発において必須となるQMS(品質管理システム)に則った設計開発の記録等がないため、大幅な手戻りが発生します。人も場所も用意が必要ですし流通経路にも気を配る必要が出てきます。どちらを選択したとしてもこれまでの広報が無に帰す(…ならよくて、マイナスリスタートとなるかも)ことになりますし、リリース時期にも遅れが発生、とほんとにいいことなしです。。
だから開発初期段階での「医療機器と非医療機器の線引きの確認」と「このアプリを医療機器とするか非医療機器とするかの判断」、大事です!

福祉用具についても述べた記事もございます。自社製品をあえて「医療機器」にしない戦略も含め、ヘルスケア市場への3つの参入ルートと成功戦略を比較検討したい方向け。
医療機器プログラム(SaMD)の開発プロセスにおける注意点
SaMDの開発プロセスにおける注意点
SaMDの開発には、一般的なソフトウェア開発とは異なる、薬機法により求められるルールがあります。
上述のプロコンの表では箇条書きでまとめていましたが、ざっと述べるとSaMDの場合、業許可と承認・認証の5年毎の更新はもちろんんですが、医療機器基本要件基準に適合させ続けること、つまり、JIS規格の改正や新たなサイバーセキュリティリスクの出現など、環境や技術の変化があった場合には、5年ごとの業許可やQMS適合性調査の更新を待つのではなく、ライフサイクル全体を通じて最新の要件に適合するよう継続的な品質・安全性の確保(アップデート等)を行うことが製造販売業者に義務付けられています。加えて、製品に何らかの変更をする場合には原則的に変更事項について、事前または事後に手続きが必要になります。
- ソフトウェア特有の「ライフサイクルプロセス」 SaMDは、開発して終わりではなく、発売後のバージョンアップやバグ修正、セキュリティパッチの適用といった継続的なメンテナンスが不可欠です。薬機法では、この開発から設計変更、廃棄に至るまでの一貫した管理プロセス(ライフサイクルプロセス)を構築し、文書化することが求められます。これは、医療機器ソフトウェアのライフサイクルプロセスの国際規格である「IEC 62304」に準拠しています。
- サイバーセキュリティ対策の重要性 ネットワークに接続されることを前提とするSaMDでは、開発の初期段階から、情報漏洩や不正アクセスを防ぐためのサイバーセキュリティ対策を設計に組み込むことが必須要件となっています。
SaMDの承認・認証申請ロードマップ
- ステップ①:該当性確認とクラス分類 まず、自社のソフトウェアがSaMDに該当するかを行政や専門家と相談し、確認します。該当する場合には、リスクに応じてクラス分類(Ⅰ〜Ⅳ)や既存の一般的名称に当てはまるものがあるかを特定します。
- ステップ②:開発プロセスの構築 前項で述べたライフサイクルプロセスに沿った開発体制を構築し、全ての工程を文書化(仕様書、テスト記録など)します。
- ステップ③:臨床・非臨床評価の実施 ソフトウェアであっても、その有効性・安全性を証明するための臨床的な評価(臨床試験データや既存の論文の活用など)や非臨床評価(性能・安全性評価試験や既存データを用いた性能評価など)が必要となる場合があります。
- ステップ④:承認・認証申請 クラス分類に応じた申請先に、サイバーセキュリティに関する資料など、SaMD特有の添付資料と共に申請を行います。
SaMD特有の新しい審査制度「IDATEN」
AIを活用したSaMDなどは、発売後もデータ学習によって性能が向上していく特性があります。しかし、従来の制度では、少しの改良でも時間のかかる「一部変更承認」が必要でした。この課題を解決するのが、IDATEN(Improvement Design within Approval for Timely Evaluation and Notice)という新しい制度です。これは、事前に変更計画の範囲を承認審査時に示しておくことで、その範囲内での改良であれば、事前の承認を不要とし、事後の届出で済むようにした画期的な仕組みです。これにより、ソフトウェアの迅速な性能向上が可能になります。
承認後の保険適用についても考えておこう
薬機法上の承認・認証を得て製品を市場に出せる段階になっても、目指す方にはもう一つ重要なステップがあります。それが「保険適用」です。医療機器事業者すべてがこれを目指すわけではありません。
- 保険適用とは? 開発したSaMDが、公的医療保険の対象となり、医療機関が患者に使用した際に診療報酬として請求できるようになるための手続きです。これがなければ、原則として自由診療(全額自己負担)でしか使えません。
- 承認とは別の手続き 薬機法に基づく承認・認証は「市場に出すための安全性・有効性の確認」ですが、保険適用は「保険診療で使うための価格や評価を決める」手続きであり、全く別のプロセスです。厚生労働省(中医協)に対して専門的な申請やヒアリングが必要となります。
- 今後の展望 保険適用のプロセスもまた専門的な知識を要します。これについては、今後のポイント解説記事で詳しく取り上げる予定です。
頼れる伴走先を見つけるのは必須
これまで述べてきたように、SaMDの開発は薬事法関係で結構ややこしいものになっています。なので餅は餅屋として、頼れるところは頼っちゃうのが現在の主流となっています。
選択肢としては以下の感じでしょうか。
- 行政に頼る
- コンサルタント(行政書士を含む)に頼る
規制当局である行政しか結局答えを持っていないので、1.行政に頼るのはいいですね。無料の相談枠もあったりします。でも相談先の選定や相談方法には少々コツがあるのも事実。でも自社のプロダクトについて個別具体的な答えを引き出す力量があるなら結局は行政に聞くしかありません。これは薬事行政に精通した人が社内にいる場合の選択肢でしょう。
規制当局の敷く中を歩いていく中で、水先案内人として2.コンサルタントに頼るのもいいと思います。コンサルタントと一口に言っても、行政による支援機関や、民間企業、個人とがあります。弊所もここに入ります。質も様々ですし、相性も様々なので、いい御縁があれば一番ですね。注意点としては、「医療機器に該当させ、承認や保険適用を目指す」方向性のサポートを得意とするコンサルタントさんも多いので(その方がコンサルタントさんにとって短期的・中長期的なビジネスとして成り立ちやすいためかな)、自社の方向性と合っているところがいいでしょう。その場合、新規性のあるプロダクトに対して、「医療機器に該当させない(非該当の)方向で進めるための回避策の提案」といったサポートの経験が薄かったり、熱意がなかったりするかもしれませんから。
行政への相談の困りどころと「通訳」の必要性
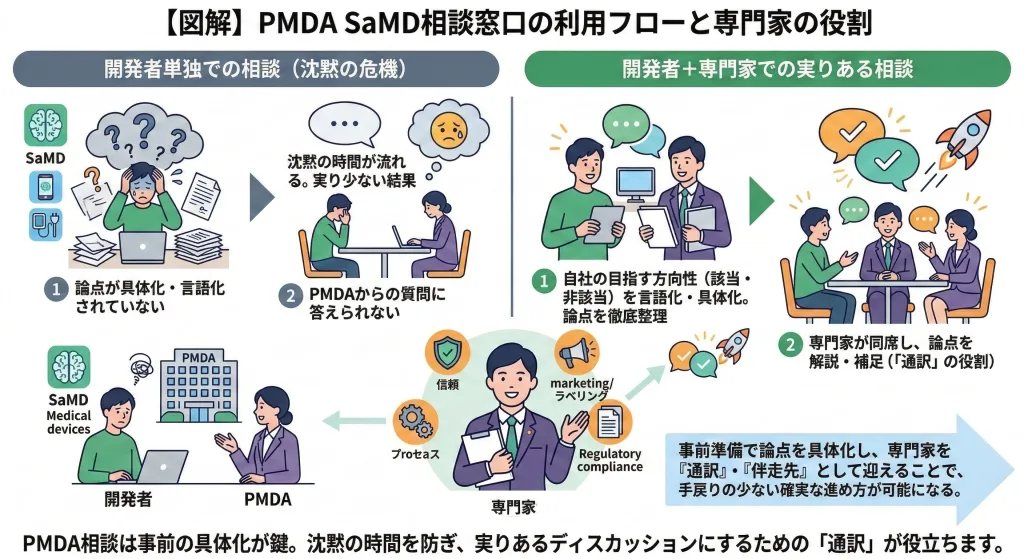
SaMDに関しては、PMDAで「SaMD一元的相談窓口」を設置しています[5]。わかりやすいですね!それに結構親切です、がやはり相談のやり方にはコツがあります。
うまく活用できないと、望んだような結果が得られず、貴重な相談時間中に沈黙が流れるといった事態にもなります。私自身も過去メーカー時代、PMDAの方との相談で「聞くことも準備してドキドキして臨んだのに、『速攻では回答できない』と言われて時間を余らせ、でも新たな質問も出てこない」という、なんとも悶えるような経験をしたことがあります。
また、相談は申し込みから実際の相談実施までに期間が空くことが通常営業です。
したがって、「自社の目指す方向性(非該当ルート含む)を理解し、PMDA相談に向けた事前の具体化や当日の通訳・安心毛布となってくれる『適切な伴走先(専門家)』を見つけて、PMDA相談を一緒に乗り切る」のが、最も手戻りが少なく確実な進め方と言えます。少なくとも私は、まさにそのエコシステム内で外部専門家として価値を提供していきたいと考えています。
つまり、SaMDの該当性は単なる「法律の分類」ではなく、開発スケジュールと事業の生死を分けるビジネスモデルの根幹です。開発を始める前の「入り口の戦略設計」と、適切な相談先の選定が不可欠です。
まとめ:手戻りを防ぐためには、開発前の「法務戦略」が必須
ヘルスケア領域におけるプログラム開発は、革新的な技術があれば成功するわけではありません。「技術」「ビジネスモデル」そして「薬機法をはじめとする法務戦略」の3つが噛み合って、初めて市場に届けることができます。
アプリの開発が進んでから「実は医療機器に該当していた」と判明した場合、数千万円単位の手戻りやリリース延期のリスクがあります。
おおぐし行政書士事務所では、貴社のアプリ企画書ベースでの「医療機器該当性・法務リスク無料確認」を実施しています。後戻りのきかない開発に着手する前に、まずは一度、専門家へ相談ください。

弊所へのご相談は初回無料・秘密厳守で承っております。まずはこちらの「お問い合わせフォームページ」からご連絡ください。
弊所の提供するヘルスケア事業支援については、「ヘルスケア支援事業ページ」にて紹介しております。ぜひご覧ください。
参考資料・参照URL
- [1] 厚生労働省.“プログラムの医療機器該当性に関するガイドライン”.厚生労働省.2023-03-31.https://www.mhlw.go.jp/content/11120000/001082227.pdf,(参照 2026-04-02).
- [2] 厚生労働省.“プログラムの医療機器該当性判断事例について”.厚生労働省.2023-03-31.https://www.mhlw.go.jp/content/11120000/001082229.pdf,(参照 2026-04-02).
- [3] 福岡県.“医療機器の販売・貸与・修理業等の許可・届出について”.福岡県.2025-01-20.https://www.pref.fukuoka.lg.jp/contents/kiki-hanbai-jouhou.html,(参照 2026-04-02).
- [4] 厚生労働省.“医薬品等適正広告基準について”.厚生労働省.2017-09-29.https://www.mhlw.go.jp/file/06-Seisakujouhou-11120000-Iyakushokuhinkyoku/0000179263.pdf,(参照 2026-04-02).
- [5] 独立行政法人 医薬品医療機器総合機構.“SaMD一元的相談窓口(医療機器プログラム総合相談)”.PMDA.2024-04-01.https://www.pmda.go.jp/review-services/f2f-pre/strategies/0011.html,(参照 2026-04-02).
【免責事項】本記事の内容は作成時点の関連法令やガイドライン等に基づく一般的な解説であり、著者個人の見解を含むものです。個別のプログラムの医療機器該当性や法的解釈を保証するものではありません。実際の開発・事業展開に際しては、所管行政機関や専門家へ個別にご相談されることをお勧めします。
お気軽にご相談ください。
- 初回相談は無料です。
- 行政書士には秘密保持の義務が課せられております。
- フォームに入力されたメールアドレス以外に、当事務所から連絡差し上げることはいたしません。
