【2026年最新】医療機器製造販売業の「三役(五役)」とは?資格要件と兼務制限の実務ガイド
はじめに
医療機器を自社ブランドで市場に流通させる「製造販売業」の許可取得において、最大の要となるのが「三役(五役)」の設置です。しかし、その設置ルールは取り扱える医療機器のリスクに応じた区分(第一種~第三種)によってなかか複雑に分かれています。
「誰がどの役職を兼ねられるのか」「実務経験は何年必要なのか」
本記事では、薬機法および最新の省令・通知に基づき、これら三役(五役)のそれぞれの役割、求められる資格、そして兼任の可否など、人的要件のポイントを根拠条文も交えながら解説します。
1. 医療機器事業の人的要件「三役(五役)」とは?
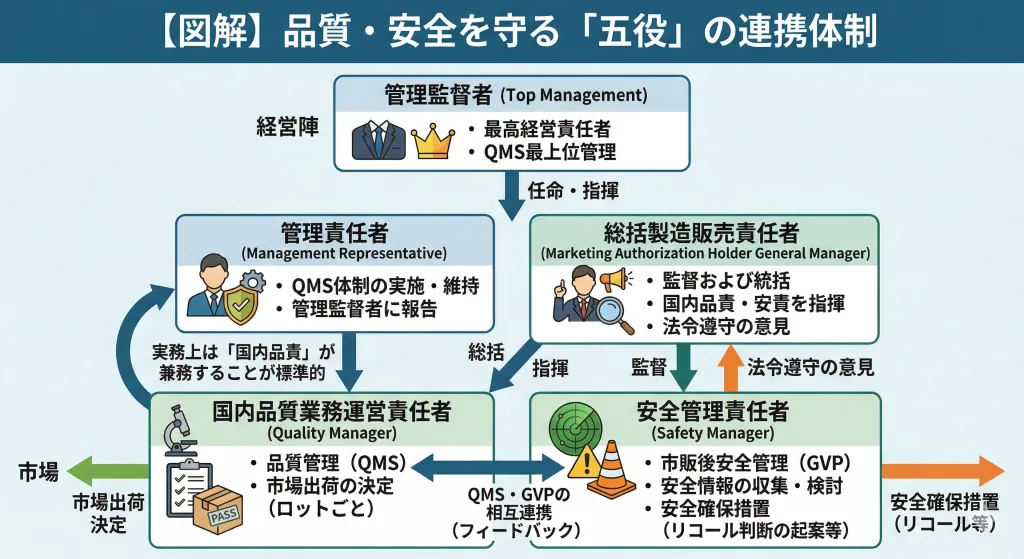
医療機器の品質管理および製造販売後安全管理を適正に行うため、医療機器の製造販売業者には以下の責任体制の構築が義務付けられています。
三役とその役割:「総責」「国内品責」と「安責」
- 総括製造販売責任者(通称:総責・総括):監督および統括 品質管理および製造販売後安全管理の業務を「統括・監督」する立場です。国内品質業務運営責任者(品責)および安全管理責任者(安責)を指揮し、法令遵守のために必要な意見を述べる義務を負います。(設置根拠法令:薬機法 第23条の2の14第1項)
- 国内品質業務運営責任者(通称:国内品責):品質管理および出荷決定 QMS省令に基づき、国内の品質管理業務を統括します。「市場への出荷の決定(出荷判定)」をロットごとに行うのは、法的にこの「品責」の役割です。(設置根拠法令:QMS省令第72条第1項)。
- 安全管理責任者(通称:安責):市販後安全管理 GVP省令に基づき、安全管理情報の収集、検討、および安全確保措置(リコール判断の起案等)の実施を統括します。(設置根拠法令:GVP省令第4条 第2項、同第13条 第2項及び同第15条において準用する第13条 第2項)。
医療機器に製販に求められる、追加の2つの役割:「管理監督者」と「管理責任者」
三役とは別に、QMS省令では「管理監督者」と「管理責任者」の設置も求めています。(QMS省令第16条)
基本的に役員等から選出されることがわかるように、QMS(品質管理監督システム)を運用するために必要な資源(リソース)を管理し、動かすことができる実行力が求められています。いずれも特定の学歴や実務経験などは要求されません。
- 管理監督者:経営陣 製造販売業者等の品質管理監督システムに係る業務を最上位で管理監督する「役員等」のことです。(根拠法令:QMS省令第2条第10項)
- 管理責任者:QMS体制の維持を担う 製造販売業者等の品質管理監督システムの実施及び維持の責任者です。管理責任者は役員、管理職の地位にある者その他これに相当する者のうち選ばれます。(根拠法令:QMS省令第16条)
2. 三役の資格要件
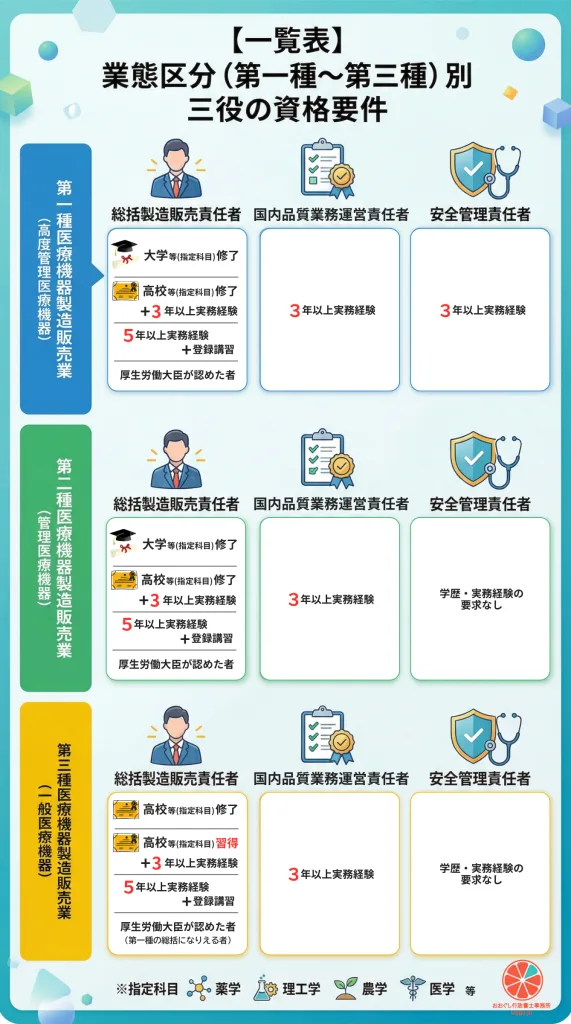
三役の要件は、扱う機器のリスク(業態区分)により異なります。特に品責の「実務経験3年」は、全クラス共通の要件である点に注意が必要です。
| 業態区分 | 扱う機器 | 総括製造販売責任者(総括) | 国内品質業務運営責任者(品責) | 安全管理責任者(安責) |
|---|---|---|---|---|
| 第一種 | 高度管理医療機器(クラス3,4) | 以下のいずれか 1. 薬剤師(※注1)又は大学等で指定科目修了 2. 高校等で指定科目修了+実務経験3年 3. 実務経験5年+登録講習修了 4. 厚生労働大臣が認めた者 | 3年以上の品質管理実務経験+能力(学歴要件なし) | 3年以上の安全確保実務経験+能力(学歴要件なし) |
| 第二種 | 管理医療機器(クラス2) | 第一種と同じ要件 | 第一種と同じ要件 | 能力を有する者(学歴要件、実務経験要求なし) |
| 第三種 | 一般医療機器(クラス1) | 以下のいずれか 1. 高校等で指定専門課程を修了 2. 高校等で指定科目を修得(履修)+実務経験3年 3. 厚生労働大臣が認めた者 (上位資格である「実務経験5年+登録講習修了」の者もこれにより第三種の総括となり得ます。) | 第一種と同じ要件 | 第二種と同じ要件 |
- (※注1)薬剤師の扱いについて: 法令上の文言は「大学等で薬学に関する専門の課程を修了した者」ですが、薬剤師はこの要件を完全に満たすため、実務上は有資格者として認められます。
- 大学等: 大学、短期大学、高等専門学校(高専)、または旧制専門学校を指します 。
- 高校等: 高等学校(工業高校等を含む)、または旧制中学校を指します 。
- 指定科目:物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学に関する専門の課程
- 総括の実務経験の範囲(第一種・第二種): 総括製造販売責任者の要件となる実務経験は、医療機器に限らず「医薬品」や「再生医療等製品」における品質管理・安全管理の経験も認められます(薬機法施行規則第114条の49第1項)。
- 総括の実務経験の範囲(第三種): 総括製造販売責任者の要件となる実務経験は、医療機器に限らず「医薬品」や「再生医療等製品」のみならず、「化粧品」や「医薬部外品」における品質管理・安全管理の経験も認められます(薬機法施行規則第114条の49第2項第2号)。
- 品責の実務経験の範囲(共通):品責の実務経験要件を定めているQMS省令(第72条第1項第2号)では、「品質管理業務その他これに類する業務に三年以上従事した者」と規定されています。総括製造販売責任者の要件のように対象品目(医薬品や医療機器など)を限定する文言がないため、化粧品や医薬部外品の品質管理経験であっても「これに類する業務」として認められます。
3. 三役および責任技術者の「兼務制限」ルール
医療機器ビジネスの体制構築において、各責任者の兼務可否はコストと人員配置に直結します。平成26年の法改正以降、業務に支障を及ぼさない範囲において、以下のような柔軟な配置が認められています。
業態区分別の三役(総括・品責・安責)兼務ルール12
製造販売業の主軸となる三役の兼務ルールは以下の通りです。第6の1]
| 業態区分 | 扱う機器 | 総括 と 品責 | 総括 と 安責 | 品責 + 安責 |
|---|---|---|---|---|
| 第一種 | 高度管理医療機器(クラス3,4) | 兼務可能 | 兼務不可 | 兼務不可 |
| 第二種 | 管理医療機器(クラス2) | 兼務可能(※) | 兼務可能(※) | 兼務不可 |
| 第三種 | 一般医療機器(クラス1) | 全員兼務可能(1名で三役すべてを兼務できます) | 全員兼務可能(1名で三役すべてを兼務できます) | 全員兼務可能(1名で三役すべてを兼務できます) |
※第二種の注意点:認められているのは「総括+品責」または「総括+安責」のいずれか一方のペアのみです。「品責+安責」を直接兼務することや、三役すべてを1名で兼務することは認められません。
【五役】および【製造所】との兼務ルール34
QMS省令上の経営層、および製造現場の責任者との兼務については、以下の通り整理されています。
- 管理監督者(最高経営責任者等):通常、社長や取締役が務めます。総括製造販売責任者を含む三役や、管理責任者との兼務に法的な制限はありません。
- 管理責任者(QMS体制の推進役):管理監督者によって任命されます。実務上は、国内品質業務運営責任者(品責)が管理責任者を兼務するケースが標準的であり、効率的な運営体制とみなされます。
- 製造所「責任技術者」:製造販売業の事務所と製造所(包装・表示・保管のみの拠点を含む)が同一の場所に所在し、業務に支障がない場合に限り、三役との兼務が可能です5。特に「品責と責任技術者」の兼務は、品質管理を一貫して行う観点から実務上も多く見られます。
第一種の兼務ルールの図
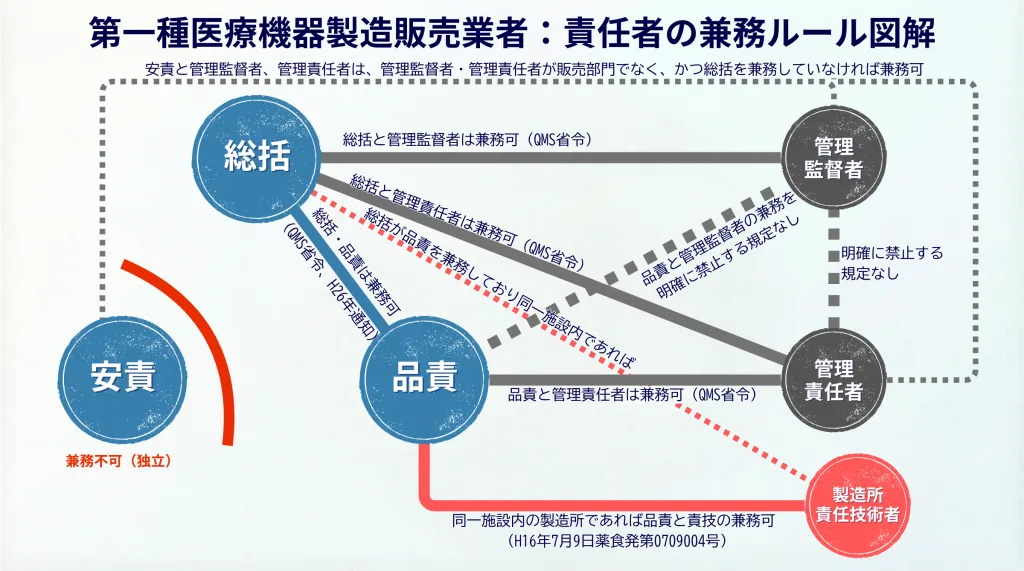
1. 第一種医療機器製造販売業で総括と品責が兼務可とするソース
- QMS省令 第71条第2項 「医療機器等総括製造販売責任者は、管理監督者若しくは管理責任者又は次条第一項に規定する国内品質業務運営責任者を兼ねることができる。」と規定されています。
- 平成26年8月6日薬食発0806第3号第6 その他 1の(1)のア 「第一種医療機器製造販売業者については、総括製造販売責任者と国内品質業務運営責任者との兼務を可能とすること」と明記されています。
2. 第一種医療機器製造販売業で、総括と管理監督者が兼務可能なソース
- QMS省令 第71条第2項 総括製造販売責任者は、管理監督者を兼ねることができる旨が規定されています。
3. 第一種医療機器製造販売業で、総括と管理責任者が兼務可能なソース
- QMS省令 第71条第2項 総括製造販売責任者は、管理責任者を兼ねることができる旨が規定されています。
4. 第一種医療機器製造販売業で、品責と管理監督者が兼務可能と判断したソース
- 品責(国内品質業務運営責任者)が単独で管理監督者を兼ねることができる旨を直接的に定めた条文は現時点で見つけられていません。
- ただし、管理監督者は「製造販売業者等の品質管理監督システムに係る業務を最上位で管理監督する役員等」と定義されており、兼任を明確に禁止する規定もありません。また、上記のQMS省令 第71条第2項により「総括が管理監督者と品責の両方を兼ねることができる」ため、結果として一人の人物(総括)が品責と管理監督者を兼務する体制は法的に認められていると解釈しております。
5. 第一種医療機器製造販売業で、品責と管理責任者が兼務可能なソース
- QMS省令 第72条第5項 「国内品質業務運営責任者は、管理責任者を兼ねることができる。」と規定されています。
6. 第一種医療機器製造販売業で、管理監督者と管理責任者が兼務可能と解釈したソース
- 兼任禁止の規定がない QMS省令において、「管理監督者」は品質管理監督システムを最上位で管理監督する「役員等」と定義され、「管理責任者」はその管理監督者によって役員や管理職等の中から任命される実務の責任者とされています。法令上、管理監督者自身が実務も担う「管理責任者」を兼ねる(自らを任命する)ことを禁止する規定は見つかっていません。
7. 第一種医療機器製造販売業で、安責と管理監督者、管理責任者が兼務可能と解釈したソース
- 安責が単独で管理監督者や管理責任者を兼ねることができる旨を直接的に定めた条文は現時点で見つけられていません。しかし兼任を明確に禁止する規定も見つけられていません。よって以下の条件を満たせば兼ねられるだろうと解釈しています。
- 「販売部門でないこと」 GVP省令により、第一種の安責は「医薬品等の販売に係る部門に属する者でないこと」と定められています。したがって、販売部門を統括するような管理監督者(役員等)や管理責任者である場合は、安責を兼務できないことは明確です。
- 「総括を兼務していないこと」 第一種において「総括」と「安責」の兼務は認められていません。そのため、管理監督者や管理責任者が同時に「総括」を務めている場合、その人物は「安責」を兼務できません。
- GVP省令で定められている「安全確保業務の適正かつ円滑な遂行に支障を及ぼすおそれがない」という大前提も満たす必要がある。
8. 同一施設内での責任技術者と第一種医療機器製造販売業の品責(・総括)の兼任可能なソース
- 平成26年8月6日薬食発0806第3号第6 その他 1の(3) 「一の法人において、製造販売業及び製造業を併せて行う場合であって、国内品質業務運営責任者がその業務を行う事務所と同一施設内に製造所を有する場合には、国内品質業務運営責任者と製造管理者又は責任技術者との兼務を可能とすること」と明記されています。
- 総括との兼任について直接触れた規定はありませんが、総括が品責を兼務できること(QMS省令第71条第2項等)を踏まえると、「品責を兼務している総括」が、上記通知の規定に基づき、同一施設内にある製造所の責任技術者を兼務することが可能となります。
第二種の兼務ルールの図
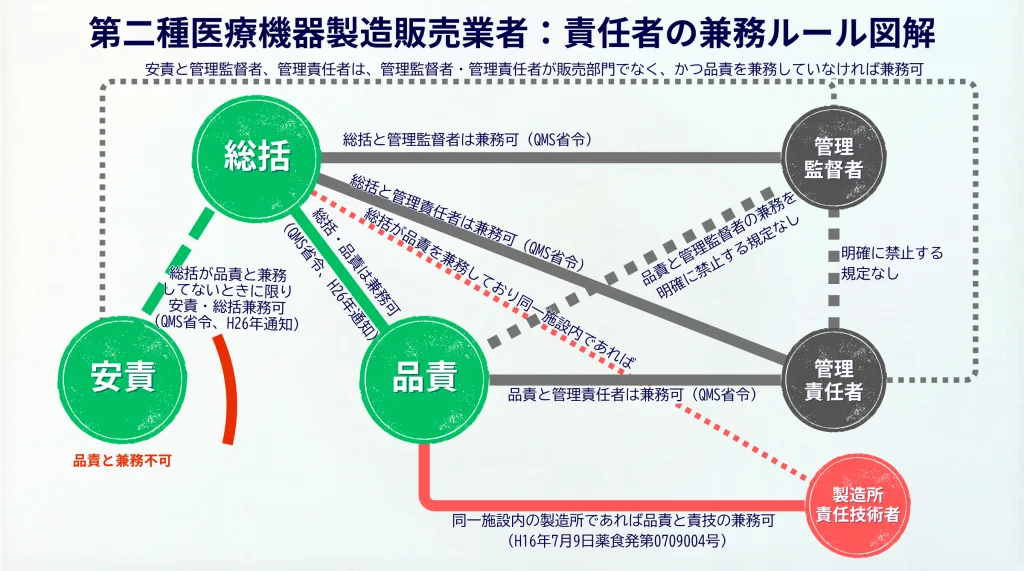
1. 第二種医療機器製造販売業で、総括と品責又は安責が兼務可とするソース
- QMS省令 第71条第2項 「医療機器等総括製造販売責任者は、管理監督者若しくは管理責任者又は次条第一項に規定する国内品質業務運営責任者を兼ねることができる。」と規定されています。
- 平成26年8月6日薬食発0806第3号第6 その他 1の(1)のイ 「第二種医療機器製造販売業者及び体外診断用医薬品製造販売業者については、総括製造販売責任者と国内品質業務運営責任者の兼務を可能とするとともに、国内品質業務運営責任者を兼務していない場合に限り、総括製造販売責任者と安全管理責任者との兼務を可能とすること」と明記されています。
2. 第二種医療機器製造販売業で、総括と管理監督者が兼務可能なソース(第一種と同じ)
- QMS省令 第71条第2項 総括製造販売責任者は、管理監督者を兼ねることができる旨が規定されています。
3. 第二種医療機器製造販売業で、総括と管理責任者が兼務可能なソース(第一種と同じ)
- QMS省令 第71条第2項 総括製造販売責任者は、管理責任者を兼ねることができる旨が規定されています。
4. 第二種医療機器製造販売業で、品責と管理監督者が兼務可能と判断したソース(第一種と同じ)
- 品責(国内品質業務運営責任者)が単独で管理監督者を兼ねることができる旨を直接的に定めた条文は現時点で見つけられていません。
- ただし、管理監督者は「製造販売業者等の品質管理監督システムに係る業務を最上位で管理監督する役員等」と定義されており、兼任を明確に禁止する規定もありません。また、上記のQMS省令 第71条第2項により「総括が管理監督者と品責の両方を兼ねることができる」ため、結果として一人の人物(総括)が品責と管理監督者を兼務する体制は法的に認められていると解釈しております。
5. 第二種医療機器製造販売業で、品責と管理責任者が兼務可能なソース(第一種と同じ)
- QMS省令 第72条第5項 「国内品質業務運営責任者は、管理責任者を兼ねることができる。」と規定されています。
6. 第二種医療機器製造販売業で、管理監督者と管理責任者が兼務可能と解釈したソース(第一種と同じ)
- 兼任禁止の規定がない QMS省令において、「管理監督者」は品質管理監督システムを最上位で管理監督する「役員等」と定義され、「管理責任者」はその管理監督者によって役員や管理職等の中から任命される実務の責任者とされています。法令上、管理監督者自身が実務も担う「管理責任者」を兼ねる(自らを任命する)ことを禁止する規定は見つかっていません。
7. 第二種医療機器製造販売業で、安責と管理監督者、管理責任者が兼務可能と解釈したソース
- 安責が単独で管理監督者や管理責任者を兼ねることができる旨を直接的に定めた条文は現時点で見つけられていません。しかし兼任を明確に禁止する規定も見つけられていません。よって以下の条件を満たせば兼ねられるだろうと解釈しています。
- 「販売部門でないこと」 GVP省令により、第一種の安責は「医薬品等の販売に係る部門に属する者でないこと」と定められています。したがって、販売部門を統括するような管理監督者(役員等)や管理責任者である場合は、安責を兼務できないことは明確です。
- 「品責を兼務していないこと」第二種では「総括+品責」または「総括+安責」のいずれか一方のペアでの兼務のみが認められており、「品責と安責」の兼務は認められていません。 そのため、もしその管理監督者や管理責任者が「品責」を務めている場合、その人物は「安責」を兼務することができません
- GVP省令で定められている「安全確保業務の適正かつ円滑な遂行に支障を及ぼすおそれがない」という大前提も満たす必要がある。
8. 同一施設内での責任技術者と、第二種医療機器製造販売業の品責(・総括)の兼任可能なソース(第一種と同じ)
- 平成26年8月6日薬食発0806第3号第6 その他 1の(3) 「一の法人において、製造販売業及び製造業を併せて行う場合であって、国内品質業務運営責任者がその業務を行う事務所と同一施設内に製造所を有する場合には、国内品質業務運営責任者と製造管理者又は責任技術者との兼務を可能とすること」と明記されています。
- 総括との兼任について直接触れた規定はありませんが、総括が品責を兼務できること(QMS省令第71条第2項等)を踏まえると、「品責を兼務している総括」が、上記通知の規定に基づき、同一施設内にある製造所の責任技術者を兼務することが可能となります。
第三種の兼務ルールの図
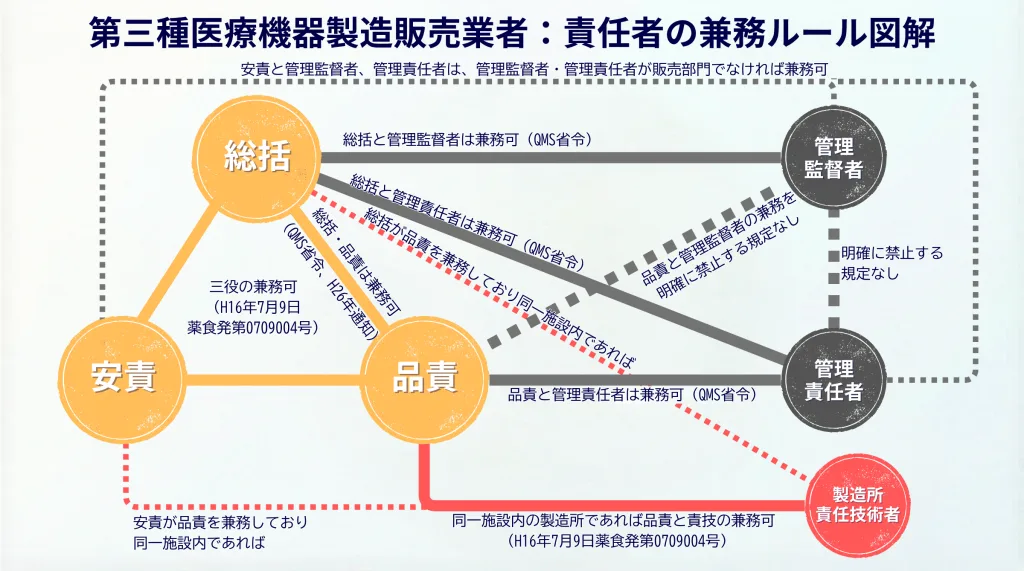
1. 第三種医療機器製造販売業で、総括と品責又は安責が兼務可とするソース
- QMS省令 第71条第2項 「医療機器等総括製造販売責任者は、管理監督者若しくは管理責任者又は次条第一項に規定する国内品質業務運営責任者を兼ねることができる。」と規定されています。
- 平成26年8月6日薬食発0806第3号第6 その他 1の(1)のウ) 「第三種医療機器製造販売業者については、総括製造販売責任者、国内品質業務運営責任者及び安全管理責任者の三者の兼務を可能とすること」と明記されています。第三種に限り、これら三役すべてを1名で兼務することが明確に認められています。
2. 第三種医療機器製造販売業で、総括と管理監督者が兼務可能なソース(第一種、第二種と同じ)
- QMS省令 第71条第2項 総括製造販売責任者は、管理監督者を兼ねることができる旨が規定されています。
3. 第三種医療機器製造販売業で、総括と管理責任者が兼務可能なソース(第一種、第二種と同じ)
- QMS省令 第71条第2項 総括製造販売責任者は、管理責任者を兼ねることができる旨が規定されています。
4. 第三種医療機器製造販売業で、品責と管理監督者が兼務可能と判断したソース(第一種、第二種と同じ)
- 品責(国内品質業務運営責任者)が単独で管理監督者を兼ねることができる旨を直接的に定めた条文は現時点で見つけられていません。
- ただし、管理監督者は「製造販売業者等の品質管理監督システムに係る業務を最上位で管理監督する役員等」と定義されており、兼任を明確に禁止する規定もありません。また、上記のQMS省令 第71条第2項により「総括が管理監督者と品責の両方を兼ねることができる」ため、結果として一人の人物(総括)が品責と管理監督者を兼務する体制は法的に認められていると解釈しております。
5. 第三種医療機器製造販売業で、品責と管理責任者が兼務可能なソース(第一種、第二種と同じ)
- QMS省令 第72条第5項 「国内品質業務運営責任者は、管理責任者を兼ねることができる。」と規定されています。
6. 第三種医療機器製造販売業で、管理監督者と管理責任者が兼務可能と解釈したソース(第一種、第二種と同じ)
- 兼任禁止の規定がない QMS省令において、「管理監督者」は品質管理監督システムを最上位で管理監督する「役員等」と定義され、「管理責任者」はその管理監督者によって役員や管理職等の中から任命される実務の責任者とされています。法令上、管理監督者自身が実務も担う「管理責任者」を兼ねる(自らを任命する)ことを禁止する規定は見つかっていません。
7. 第三種医療機器製造販売業で、安責と管理監督者、管理責任者が兼務可能と解釈したソース
- 第三種では「総括・品責・安責の三者の兼務」が認められており、かつ総括は管理監督者および管理責任者を兼務できるため、「総括・品責」を兼任している安責であれば、明文規定に基づいて管理監督者や管理責任者を兼務することが可能となります。
- 安責が単独で管理監督者や管理責任者を兼ねることができる旨を直接的に定めた条文は現時点で見つけられていません。しかし兼任を明確に禁止する規定も見つけられていません。よって以下の条件を満たせば兼ねられるだろうと解釈しています。
- 「販売部門でないこと」 GVP省令により、第一種の安責は「医薬品等の販売に係る部門に属する者でないこと」と定められています。したがって、販売部門を統括するような管理監督者(役員等)や管理責任者である場合は、安責を兼務できないことは明確です。
- GVP省令で定められている「安全確保業務の適正かつ円滑な遂行に支障を及ぼすおそれがない」という大前提も満たす必要があります。
8. 同一施設内での責任技術者が、第三種医療機器製造販売業の総括や品責、安責と兼任可能なソース
- 品責との兼任について:平成26年8月6日薬食発0806第3号第6 その他 1の(3) 「一の法人において、製造販売業及び製造業を併せて行う場合であって、国内品質業務運営責任者がその業務を行う事務所と同一施設内に製造所を有する場合には、国内品質業務運営責任者と製造管理者又は責任技術者との兼務を可能とすること」と明記されています。
- 総括や安責との兼任について:「総括」や「安責」という役職単独で責任技術者との兼務を認める直接的なソースはありませんが、前述の通り第三種では「総括・品責・安責」の三役すべての兼務が可能とされています。そのため、第三種で三役を兼ねている人物であれば、上記の通知に基づく「品責」としての要件を満たすため、同一施設内にある製造所の責任技術者を兼任することが(結果的に)可能となるだろうと解釈しています。
直接雇用と常勤性の要求
兼務が認められる場合であっても、薬機法上の責任者には「実態を伴う適正な管理」が求められます。他社での常勤職との掛け持ちや、名義貸しは重大な違反となります。
- 直接雇用の原則:責任者は原則として、自社の役員または正社員(直接雇用)である必要があります。派遣社員や外部コンサルタントを責任者に据えることはできません。
- 常勤性の要求:各責任者はその事業所に常勤し、実質的な管理監督を行う必要があります。名義貸しや、他社での常勤職との掛け持ちは、重大な薬機法違反となるリスクがあります。
- 専念義務:他社での常勤職との掛け持ちは、自社業務への専念義務および常勤性の観点から原則として認められません。
なぜ薬機法はこれほどまでに「直接雇用」と「常勤性」を求めるのでしょうか?その法的背景と、実務上の注意点については以下の解説記事をご確認ください。

なぜ薬機法はこれほどまでに「直接雇用」と「常勤性」を求めるのでしょうか?その法的背景と、実務上の注意点については以下の解説記事をご確認ください。
4. まとめ
医療機器製造販売業の体制構築は、単なる「人数合わせ」ではありません。扱う機器のリスクに応じた適正な兼務制限と、正確な実務経験・講習要件の確認が不可欠です。
おおぐし行政書士事務所では、貴社の製品クラスと人的リソースに基づき、法令を遵守した最短の体制構築をサポートいたします。許可申請前の要件チェックは、ぜひ当事務所の無料相談をご活用ください。
参考(参考文献・関連URL)
- 厚生労働省医薬食品局長.“薬事法等の一部を改正する法律等の施行等について(平成26年8月6日付け 薬食発0806第3号 厚生労働省医薬食品局長通知)”.厚生労働省.2014-08-06. ↩︎
- 平成16年7月9日付け 薬食発第0709004号 厚生労働省医薬食品局長通知 第26の1の(3) 「国内品質業務運営責任者がその業務を行う事務所と同一施設内に製造所を有する場合には、国内品質業務運営責任者と製造管理者又は責任技術者との兼務を可能とすること」の根拠 ↩︎
- QMS省令 第71条第2項「医療機器等総括製造販売責任者は、管理監督者若しくは管理責任者又は次条第一項に規定する国内品質業務運営責任者を兼ねることができる」 ↩︎
- QMS省令 第72条第5項 「国内品質業務運営責任者は、管理責任者を兼ねることができる」 ↩︎
- 保管のみを行う拠点を含む点に関する最新の根拠: 令和3年4月28日付け 薬生薬審発0428第2号 厚生労働省医薬・生活衛生局医薬品審査管理課長通知 記の3の(4) (保管のみを行う製造所の責任技術者の兼務についても、上記の平成16年施行通知の通りに行うことと明記されています) ↩︎
お気軽にご相談ください。
- 初回相談は無料です。
- 行政書士には秘密保持の義務が課せられております。
- フォームに入力されたメールアドレス以外に、当事務所から連絡差し上げることはいたしません。
