【2026年完全版】大麻由来製品(CBD/CBN)輸入・販売ガイド:成分規制への移行と実務
【更新】 本記事は、この記事は2022年6月に公開されたものですが、2023年12月6日に成立した「大麻取締法及び麻薬及び向精神薬取締法の一部を改正する法律(令和5年法律第84号)」の段階的施行、および、最新のΔ9-THC残留限度値の適用、さらには直近の指定薬物に関する「改正省令」の動向(2026年現在)に対応し、内容を大幅に加筆・修正を行いました。

これまでの法改正と段階的な施行、そしてこれから…。
2026年現在、日本のカンナビノイド規制はなかなか安定しない状態が続いています。この背景には、以下のスケジュールで進められた法改正の段階的施行[1]と、別軸で進行する直近の省令改正があります。
- 法改正の第一段階施行(2024年12月12日): 長らく議論の的となっていた「大麻草の成熟した茎や種子から抽出したか否か」という形式的な部位規制が撤廃され、THCの成分規制(定量規制)へと完全移行しました。
- 法改正の第二段階施行(2025年3月1日): 栽培免許の区分見直しなどを含む新制度が本格稼働しました。
- 直近の省令改正(2026年3月中下旬公布予定): 上記の法改正とは別に、薬機法に基づく指定薬物部会の審議により、CBNを新たに指定薬物に追加して省令改正する方向性が決定されました[2]。改正省令はパブコメを[3]経て、公布日は3月中下旬、施行日は6月1日の予定です[4]。
というわけで、現在は大麻由来か否かにかかわらず、製品の形状ごとに定められた残留限度値を超えてTHCが検出された製品は「麻薬」として厳しく取り扱われています[5]。さらに、本年6月予定の改正省令の施行以降は、CBNを含有する製品も原則製造、輸入、販売、所持、使用等が禁止となります。事業者が対応しなくちゃいけないことはどんどん増えていってる状況ですね。
【前提知識】大麻由来成分(カンナビノイド)と指定薬物の関係性
具体的な法規制の実務に入る前に、まずは市場で流通する主要な成分の違いと、「指定薬物」という法的な枠組みについて整理しておきましょう。
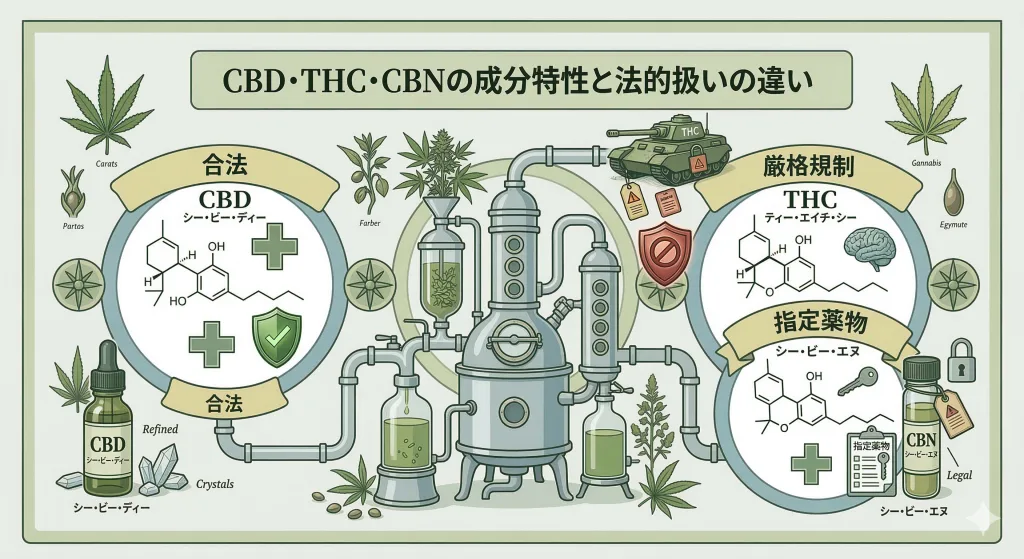
1. CBD、THC、CBN等の関係性
大麻草に含まれる100種類以上の化学物質の総称をカンナビノイドと呼びます。日本で製品を流通させようとする場合には、以下の3つの成分を押さえておく必要があります。
- THC(テトラヒドロカンナビノール): 日本の法律において麻薬として厳しく規制されている対象のひとつであり、製品への残留は極微量(後述の残留限度値)しか許されません。『大麻の有害作用を引き起こす主な成分はΔ9-THCである。このΔ9-THCが脳内のカンナビノイド受容体に結合し、神経回路を調整することにより作用が発現する。』および『大麻を長期間乱用することにより、記憶や認知に障害を及ぼし、さらに精神障害を発症するなどの健康被害を生じる危険性がある。』とされています[6]。
- CBD(カンナビジオール): THCが基準値以下であれば合法的に輸入・販売が可能です。日本のカンナビノイド市場の主役とも言えるでしょうね。『CBD(カンナビジオール)は、THCのような中枢神経作用がないとされている成分であり』とされています[6]。
- CBN(カンナビノール): 『精神毒性を有する蓋然性が高く、かつ、人の身体に使用された場合に保健衛生上の危害が発生するおそれがある物』と公式に認定されました[4]。これにより、新たに指定薬物として厳格に規制されることとなりました。
2. 「指定薬物」とは何か?
指定薬物とは、「医薬品医療機器等法(薬機法)」に基づく規制枠組みです。中枢神経系への作用(精神毒性など)を有する蓋然性が高く、健康被害が発生するおそれがある物質を、厚生労働省が指定します[7]。
- 規制の目的: いわゆる「危険ドラッグ」や「脱法ハーブ」など、次々と現れる精神作用物質を迅速に規制するためのモグラ叩き的な制度です。
- 指定された場合の効果: 医療等の正規の目的を除き、製造、輸入、販売、所持、使用が全面的に禁止され、違反すれば厳しい刑事罰の対象となります。今回、CBNがこのリストに追加されることになります。
これらの前提を踏まえた上で、事業者が直面する法務・実務上のポイントを解説します。
1. 【大麻取締法・麻向法】部位規制から「成分規制」への転換
日本のカンナビノイド市場をめぐる法規制は、2024年から2025年にかけての法律の段階的施行を経て大きく姿を変えました。適法性の判断軸がどのように変わったのかを整理します。
① 第一段階施行(2024年12月12日):成分規制の開始
長らく、大麻由来製品の適法性は「大麻草の成熟した茎や種子から抽出したか否か」という形式的な部位規制によって判断されていました。しかし、この第一段階施行により部位規制は完全に撤廃されました[1]。代わって導入されたのが、製品中にΔ9-THCがどれだけ含まれているかで適法性を判断する成分規制(定量規制)です。
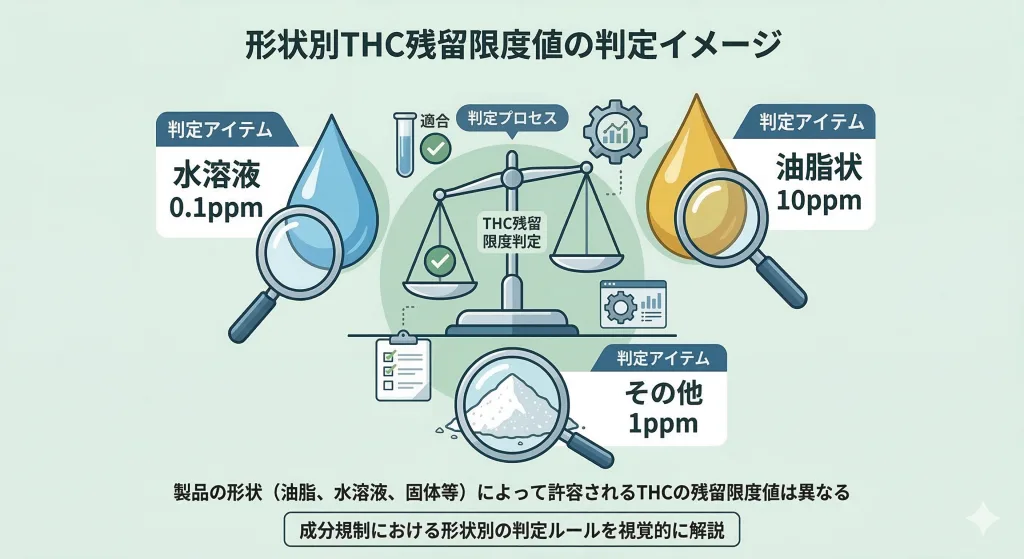
【判定マトリクス】成分規制におけるTHC残留限度値と製品形状
成分規制の根幹となるのが、以下のΔ9-THC残留限度値です。抽出部位にかかわらず、国が定めたこの基準値を超えてTHCが検出された製品は、「麻薬」として摘発されます。判定は、製品の通常の使用状態を想定し、原則として15〜25℃の常温下で行われます[5]。
| 製品の形状 | THC残留限度値(重量比) | 該当製品の例 |
|---|---|---|
| 油脂状(液体)、粉末 | 10ppm (0.001%) | CBDオイル、MCTオイル混合液、ベイプリキッドなど |
| 水溶液 | 0.1ppm (0.00001%) | CBD飲料、水溶性リキッドなど |
| その他 | 1ppm (0.0001%) | CBDアイソレート、グミ、タブレット、ワックスなど |
【事実と根拠】なぜこの数値なのか? この残留限度値は、大麻規制検討小委員会で示された「THCの精神作用が出ない量よりもさらに安全性を高く見積もること」「違法な大麻使用を調べる尿検査に影響を与えないこと」という方向性に基づいて設定されました。 具体的には、一般の事業者が輸入・販売できる食品等の基準として、THCの作用が出る製品が市場に出回らないよう、2015年に欧州食品安全機関が示したガイドライン(急性参照用量)を参考にしています。これに、製品の区分(形状)ごとに人がどれくらい摂取するかを考慮して計算し、最終的な数値を決定しています[8]。
注意: 基準値は「検出限界(LOD)」ではありません。「製品中に含まれる絶対量」の閾値です。
② 第二段階施行(2025年3月1日):栽培免許区分の見直しと新制度の稼働
「大麻取締法」は「大麻草の栽培の規制に関する法律」へと名称が変更され、栽培に関する新制度が本格稼働しました。具体的には、栽培免許が「第一種(産業用:繊維や種子など)」と「第二種(医療用・研究用など)」に明確に区分されました。これにより、適切な管理下での国内栽培や医療・産業用途での適正な活用が促進される一方で、流通経路の追跡(トレーサビリティ)や厳格な在庫管理など、事業者には従前よりも高いコンプライアンス意識と管理体制が求められるようになっています。
2. 【薬機法】CBN等の指定薬物化(直近の省令改正)
大麻取締法の改正(成分規制への移行)に加えて、厚生労働省の薬事・食品衛生審議会(指定薬物部会)における省令改正も実務に影響を及ぼす大変化です。
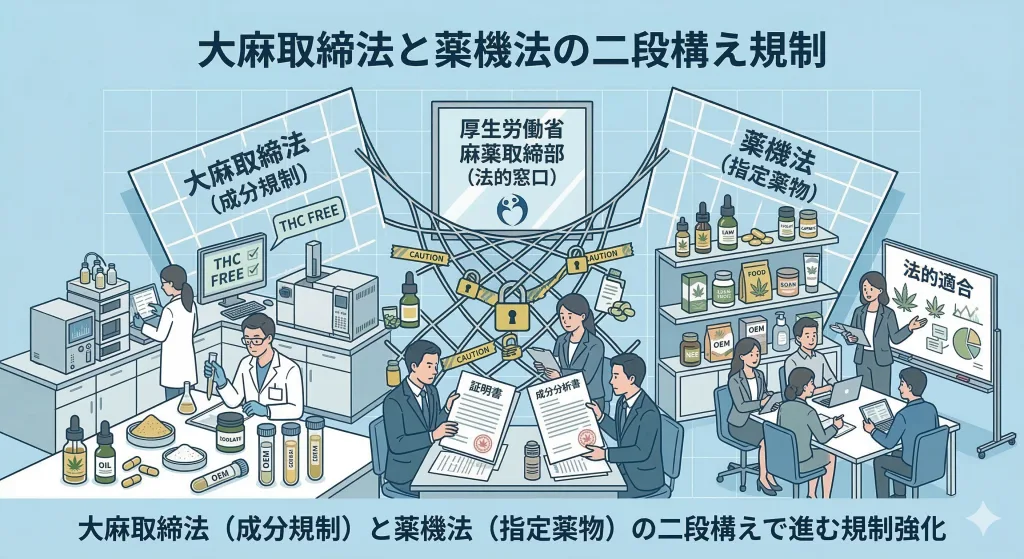
① 二段構えの規制:法改正とは別軸で進む指定薬物化
二段階に分かれてやってきた法改正の波をようやくやり過ごした、というところで、今度は省令改正です。認識のアップデート、がんばりましょう…! この省令改正(CBN等の指定薬物化)は、上述した「令和5年法律第84号」による大麻取締法の改正の流れとは全く別の枠組みで行われています。
- 大麻取締法の改正: 大麻草全体に関するルール変更(部位規制からTHC成分規制への移行)。
- 薬機法に基づく指定薬物化: 「医薬品医療機器等法(薬機法)」という別の法律に基づき、危険な物質を個別に審査し、「指定薬物」リストに追加して取り締まる定常的なプロセス。
大麻取締法が改正され、THC残留基準さえ守れば合法的なカンナビノイド製品(CBD等)が流通しやすくなった一方で、指定薬物リスト入りしたカンナビノイド(CBN)についても要配慮!ってことですね。つまり、THCの残留限度値をクリアしている製品であっても、新たに指定薬物に追加された成分(CBN等)が混入していれば、即座に違法(薬機法違反等)として摘発の対象となるってことです。
② CBNの現状と今後のスケジュール
CBDに次ぐ勢いで市場に流通していたCBNについては、この指定薬物化の対象となり、法的なステータスが大きく転換します。
- 指定薬物化の決定: 厚生労働省の「薬事・食品衛生審議会 指定薬物部会」において、CBNは「精神毒性を有する蓋然性が高く、かつ、人の身体に使用された場合に保健衛生上の危害が発生するおそれがある物」であることが認められました。
- 今後のスケジュール: これを受け、CBNを指定薬物に追加する「改正省令」が3月中下旬に公布され、6月1日に施行される予定です。
- 難治性疾患患者への特例的対応: 指定薬物化に伴い、パブリックコメント等での意見も踏まえ、CBNを継続使用せざるを得ない難治性疾患患者のための特例的な手続き(診断書の提出など)が行政より案内されています。医療目的での取り扱いは厳格なルールの下で管理されます。
- 実務への影響: 6月1日の施行以降、嗜好品としてのCBN製品の製造、輸入、販売、所持、使用は違法(指定薬物としての規制対象)となります。また、カンナビノイド原料は抽出・精製過程で他の成分が残留・変化しやすいため、CBD製品を扱う際にも、指定薬物(CBNや合成カンナビノイド等)が混入していないか、COAでの確認が従前以上に厳しく求められます。

※CBDを用いた化粧品の輸入手続き全般については、『「海外化粧品を輸入して売りたい!」実務ガイド:基礎知識編』もあわせてご確認ください。
3. 実務の急所:COA(成分鑑定書)の精査と分析手法の信頼性
規制の枠組み(THC基準と指定薬物リスト)を理解した上で、事業者が輸入・販売の実務において最も注意すべきなのは、成分鑑定書(COA)の信頼性です。
① COAに潜む「LOD / LOQ(検出・定量限界)の罠」
行政機関(厚生労働省麻薬取締部や税関)の審査において、「THC 0%」や「ND(Not Detected = 不検出)」と記載された海外メーカーのCOAを提出したにもかかわらず、輸入が差し止められるケースは実は、あります。
- LODとLOQの決定的な違い: ここで知っておくといいのが、LOD(Limit of Detection:検出限界)とLOQ(Limit of Quantitation:定量下限値)の違いです。両者はアルファベットの並びが似てるので紛らわしいんですが、訳文で書くと違いがわかりやすいですね。日本にCBD関連製品を輸入する際には基本的にLODとLOQのどちらも値が記載されていることが必要です[5]。
- LOD(検出限界): 「成分が存在するかどうか」をかろうじて検出(判断)できる最小濃度。
- LOQ(定量下限値): 「どれくらいの量が含まれているか」を正確に測定(定量)できる最小濃度。(通常、LODよりも数倍高い数値になります)
- なぜ「THC ND」でも輸入が止まるのか: 私が接した案件では、原因は、COAを作成した検査機関の「分析感度(LOQやLOD)」が日本の規制値よりも高い(粗い)ことがありました。メーカーが「LOD基準でのND(検出されず)」をアピールするのはままあるんですが、日本の行政(厚労省)が厳格に求めているのは「規制値以下であることを正確に証明できる定量性(LOQが基準値未満であること)」です。
- 事例(例です!): 例えば、日本の基準が 0.1ppm の水溶液(CBD飲料等)に対し、提出されたCOAのLOQ(あるいはLOD)が 1ppm だった場合。LODが1ppmでの「ND」は、「1ppm以上は含まれていない」ことを意味するだけであり、「0.1ppm〜0.9ppmの範囲でTHCが含まれている可能性」を排除できません。
- 行政の判断論理と対策: 行政手続上、事業者は「基準値(0.1ppm)を下回っていること」を立証する責任があります。したがって、事業者は海外メーカーに対し、日本の規制値に対して十分な感度(LOQが少なくとも規制値と同等か、推奨は1/10以下)を持つ検査機関での測定を粘り強く要求する必要があります。(実際のところ、後でごねても「できないものはできない」と突っぱねられやすいので、最初の商談の時点で「この規制値で行けるよね?」と詰めておきましょう。COAの例をもらいましょうね!契約書にもできるだけ反映させましょうね!)
② 分析手法の信頼性:なぜ「LC-MS/MS」が求められるのか
法改正後の製品中のTHCの残留限度値は極微量ですよね。それをどうやって測って基準値以下であることを証明すればいいのか。これについては厚労省は親切にも文書を作って例示してくれています[9]。
この文書では定量の分析手法として「LC-MS/MS」と「LC-QTOF MS」を提示しています。今までの定番はHPLC-UVだったんですけど、0.1ppmレベルとかになってくると、HPLC-UVでは感度と特異性を担保できないんでしょうね。
この例示についてのパブコメ[10]には「1ppm 又は 0.10ppm のΔ9-THC を測れる分析機器としては、精密質量分析装置(MS/MS 等)を使用するものになると想定しております」との記述がありましたし、この例示の策定のための研究[11]ではHPLC-UVは候補にも上がっていないですし…。
- THCだけでなく「THCA(酸性体)」も合算して測る根拠: 同通知において、分析対象化合物にはTHCだけでなく「$\Delta^9$-THCA-A(THCの酸性体)」も明記されました。THCA自体には精神作用がなくても、熱や光が加わることで容易に「THC」に変化(脱炭酸)してしまうため、「製品中のTHC量」と「THCA-AをTHCに換算した量」の総量で評価しなければ安全性が担保できないという科学的根拠に基づいています。
- 分析法を「決定」ではなく「例示」とした理由: パブリックコメントの段階では、業界から「基準値が低すぎて対応できる検査機関がない」「コストがかかる」といった懸念が多く寄せられました。また、研究段階でも、製品の形状や混ざっている他の成分によって、うまく抽出できなかったり分析の邪魔になったりする課題がありました。 そのため厚労省は、「これが絶対のルール」とするのではなく、「代表的な製品形態で精度が担保できた方法を示す」という「例示」という形を取りました。つまり、同等以上の特異性・定量性が担保できるのであれば、他の分析法を適用することも妨げない、という実務に配慮した柔軟な着地となっています。
総じて、海外メーカーから安価なHPLCによる分析結果を提示されたとしても、日本の行政機関の厳格な審査に耐えうる証明を行うためには、LC-MS/MS等を用いた「THCとTHCAの総量」の信頼できる分析データを取得することが、現在の実務における絶対のスタンダードとなっています。というわけで、法的リスクを低減するためには、LC-MS/MS(またはGC-MS/MS)による信頼性の高い分析データこそが不可欠です。
4. まとめ:正しく選択し、正しく実行する

段階的な法改正(成分規制への完全移行)および、直近の省令改正(CBNの指定薬物化)により、大麻由来製品ビジネスは「知らなかった」や「メーカーが大丈夫と言っていた」では済まされない、高度な法務・科学的リテラシーが求められる領域に入りました。
- 二段構えの規制を理解する(大麻取締法のTHC基準値クリアだけでなく、薬機法による指定薬物リストも注視する)。
- 形状ごとの基準値を再確認する(常温15〜25℃下での状態判定)。
- COAのLOD/LOQ(検出・定量限界)を精査する(行政の立証責任に耐えうるか)。
- 分析手法の信頼性を担保する(HPLCを退け、LC-MS/MSのデータを取得する)。
- 指定薬物のスケジュールを厳守する(CBNの改正省令公布と6月1日施行に向けた対応)。
基準値を超えた製品の輸入・所持や、指定薬物の販売は、「麻薬及び向精神薬取締法」または「医薬品医療機器等法」違反として逮捕・摘発に直結します。自社の事業が「砂上の楼閣」になっていないか、今一度、科学的エビデンスの徹底した精査を行ってください。
実務的な課題や成分チェックのご相談
一般消費者が日本で通常入手できるCBD製品は様々な形態がありますが、いずれも基本的には化粧品、雑品あるいは医薬品、食品のいずれかに振り分け可能です。
それらはそれぞれ日本で流通させるまでの手続きが違います。そうです。THCと指定薬物をクリアしても、まだ手続きあるんですよ…。
うちの製品どのルートを選択できる?各ルートのメリット・デメリットは?悩ましいですよね。
せっかくの良い製品なのなら、胸を張って消費者に届けることができるよう、しっかり製品区分ごとの規制も押さえて販売に至っていただきたいです。
特に、ようやく日本で広がりを見せ始めた大麻由来製品群では、法的にクリーンであることは未来の市場のためにも重要です。
弊事務所では、ヘルスケア製品にかかるお手続き支援を幅広く取り扱ってございます。
事業者さんのルート判断材料を取り揃えるための調査も承っております。
最初の面談は無料ですので、企画段階からでも、手元に製品出来上がっていても、どうぞお気軽にご連絡ください。

参考(参考文献・関連URL)
本記事は、以下の根拠に基づき構成しています。
- 「令和7年3月1日に「大麻取締法及び麻薬及び向精神薬取締法の一部を改正する法律」の一部が施行されます(厚生労働省ウェブサイト)」, 3月 12, 2026にアクセス、 https://www.mhlw.go.jp/stf/newpage_43079.html
- 「2025年10月28日 薬事審議会 指定薬物部会 議事録(厚生労働省ウェブサイト)」, 3月 12, 2026にアクセス、 https://www.mhlw.go.jp/stf/newpage_65649.html
- 「「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第二条第十五項に規定する指定薬物及び同法第七十六条の四に規定する医療等の用途を定める省令の一部を改正する省令案」に関する意見募集について」, 3月 12, 2026にアクセス、 https://public-comment.e-gov.go.jp/servlet/Public?CLASSNAME=PCMMSTDETAIL&id=495250249&Mode=0
- 「薬物乱用防止に関する情報(厚生労働省ウェブサイト)」, 3月 12, 2026にアクセス、 https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/iyakuhin/yakubuturanyou/index.html
- 「CBDオイル等のCBD関連製品の輸入について(麻薬取締部ウェブサイト)」, 3月 12, 2026にアクセス、 https://www.ncd.mhlw.go.jp/cbd.html
- 「大麻規制のあり方に関する大麻規制検討小委員会 議論のとりまとめ(厚生労働省ウェブサイト)」, 3月 12, 2026にアクセス、 https://www.mhlw.go.jp/content/11126000/001272787.pdf
- 「指定薬物について(厚生労働省ウェブサイト)」, 3月 12, 2026にアクセス、 https://www.mhlw.go.jp/bunya/iyakuhin/yakubuturanyou/scheduled-drug/index.html
- 「大麻取締法及び麻薬及び向精神薬取締法の一部を改正する法律の施行に伴う関係政令の整備に関する政令案に関する意見募集の結果について」, 3月 12, 2026にアクセス、 https://public-comment.e-gov.go.jp/pcm/download?seqNo=0000279560
- 「令和6年11月12日 医薬監麻発1112第3号 大麻草由来製品等に含まれるΔ9-THC の残留限度値に係る分析法の例示について」, 3月 12, 2026にアクセス、https://www.mhlw.go.jp/content/11120000/001330798.pdf
- 「大麻由来製品に含まれるΔ9-THC の標準的な分析法案に関する意見募集の結果について」, 3月 12, 2026にアクセス、https://public-comment.e-gov.go.jp/pcm/download?seqNo=0000282583
- 「厚生労働科学特別研究事業 大麻由来製品中に混在する微量Δ9-THC の試験法策定に資する研究 令和5年度 総括・分担研究報告書」, 3月 12, 2026にアクセス、https://mhlw-grants.niph.go.jp/system/files/download_pdf/2023/202306026A.pdf
お気軽にご相談ください。
- 初回相談は無料です。
- 行政書士には秘密保持の義務が課せられております。
- フォームに入力されたメールアドレス以外に、当事務所から連絡差し上げることはいたしません。