日本で流通が禁止される化粧品とは:化粧品基準から品質保証の試験検査まで
ほとんどの消費者は、日本国内で一般に販売されている化粧品は、安全なものだろうと無意識に信頼しています。その魅力的なコンセプトや使用感の裏側には、事業者の絶え間ない努力によって支えられる、科学的根拠に基づいた安全性と品質の確保という大前提が存在します。
この安全性と品質は、どのように担保されるのでしょうか。まず、製造業者は原料の選定や情報の精査、製造工程のメンテナンス、各種試験などを通じて、安全な製品を作る体制を整えます。そして、その製品の最終責任を負う製造販売業者は、こうした製造業者の活動を管理・監督することによって製品の品質と安全性を保証し、自社の名前で市場に流通させます。海外から製品を輸入する場合も同様で、海外の法律と日本の法律は異なるため、日本の市場で流通させる製品については、日本の法規制に適合する形で品質・安全性を確保することが製造販売業者には求められます。
この記事では、この「品質・安全性の確保」の根幹にある、日本の化粧品に対する成分規制と、それをクリアしていることの確認としての試験検査について、その目的と内容を解説します。
1.日本における「流通禁止の化粧品」とは
日本における化粧品の規制は、すべからく薬機法に根拠があります。成分規制も薬機法の根拠から見ていってみましょう。
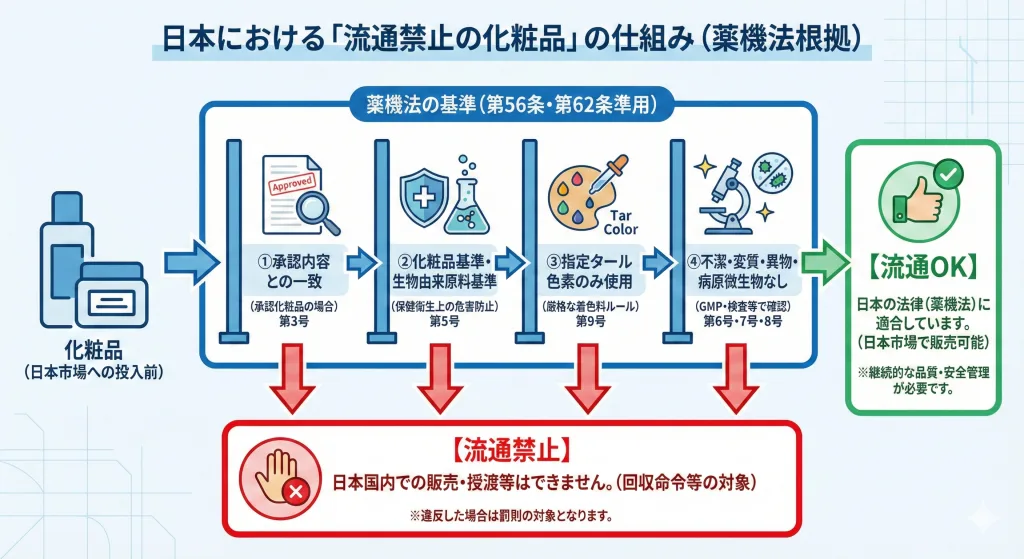
薬機法には以下のような定めがあります(第56条を第62条で準用)。有り体に言うならば、「この各号のどれかにあてはまる化粧品は、日本で販売、授与、製造、輸入、貯蔵、陳列等しちゃいけない、適合してなきゃダメな基準等リスト」です。
(販売、製造等の禁止) 第五十六条を第六十二条で準用 次の各号のいずれかに該当する化粧品は、販売し、授与し、又は販売若しくは授与の目的で製造し、輸入し、貯蔵し、若しくは陳列してはならない。 (中略) 三 第十四条又は第十九条の二の承認を受けた化粧品であつて、その成分若しくは分量(成分が不明のものにあつては、その本質又は製造方法)又は性状若しくは品質がその承認の内容と異なるもの(第十四条第十六項(第十九条の二第五項において準用する場合を含む。)の規定に違反していないものを除く。) 四 第十四条第一項の規定により厚生労働大臣が基準を定めて指定した化粧品であつて、その成分若しくは分量(成分が不明のものにあつては、その本質又は製造方法)又は性状若しくは品質がその基準に適合しないもの 五 第四十二条第二項の規定によりその基準が定められた化粧品であつて、その基準に適合しないもの (中略) 九 着色のみを目的として、厚生労働省令で定めるタール色素以外のタール色素が使用されている化粧品
で、化粧品に関するもののみを抽出してみると、各号を根拠条文とする基準は以下のようになります。
- 第3号を根拠とする:承認内容(承認化粧品の場合に限る):新成分配合などで個別に「承認」を得た化粧品が、その承認内容と異なる場合に適用されます。
- 第5号を根拠とする:化粧品基準(第42条第2項根拠):保健衛生上の危害を防止するために設けられた制限です。
- 第5号を根拠とする:生物由来原料基準(第42条第2項根拠):動物由来原料などを使用する場合の基準です。
- 第9号を根拠とする:医薬品等に使用することができるタール色素を定める省令:着色料に関する厳格なルールです。
加えて以下はGMPや検査等で確認することになるでしょう。
- 第6号を根拠とする:その全部又は一部が不潔な物質又は変質若しくは変敗した物質から成っていないこと
- 第7号を根拠とする:異物が混入し、又は付着していないこと
- 第8号を根拠とする:病原微生物その他疾病の原因となるものにより汚染され、又は汚染されているおそれがないこと
つまり、上記の項目すべてをクリアしていることの確認が、「薬機法に定められた禁止された化粧品に該当しない」ことの確認となっていくわけです。
2.各基準について
①承認内容と一致すること(承認化粧品の場合に限る)

実は、化粧品のほとんどは届出だけで販売できるのですが、中にはあらかじめ厚生労働大臣の「承認」を得なければならない特別なものがあります(薬機法第14条第1項)。これを「承認化粧品」と呼びます。具体的にどんなものが承認対象なのか、は平成12年9月厚生省告示第330号「薬事法第14条第1項の規定に基づき厚生大臣の指定する化粧品の成分を定める件」に示されています。
現在の化粧品の多くは、後述する「化粧品基準」の範囲内であれば届出(通知)のみで販売できる「通知品目」が主流ですが、一部の特殊な処方や新成分については、国による個別の審査が必要になります。このルートの場合、単に一般的な基準を守るだけでなく、「個別に承認を受けた成分・分量・製法」と、流通させる製品実物が違わず一致していることが求められます。
②化粧品基準(平成12年厚生省告示第331号)
薬機法第56条第5号から化粧品基準を導く
第62条で準用した薬機法第56条第5号に記載されている第42条は以下の条文です。
(医薬品等の基準)
第四十二条 略
2 厚生労働大臣は、保健衛生上の危害を防止するために必要があるときは、医薬部外品、化粧品又は医療機器について、薬事審議会の意見を聴いて、その性状、品質、性能等に関し、必要な基準を設けることができる。
この薬機法第42条第2項の規定に基づき、保健衛生上の危害を防止するために、化粧品について「化粧品基準」と「生物由来原料基準」が設けられているわけです。つまりこれらは法に定められた制限なんですね。しっかり守りましょう。
化粧品基準の内容
化粧品基準(厚生省告示第331号)(厚労省が公開している化粧品基準へのリンク)は、以下の要素で構成されています。
- 総則:安全性の基本原則/ 化粧品基準の最も基本的な考え方として、「化粧品の原料は、それに含有される不純物等も含め、感染のおそれがある物を含む等その使用によって保健衛生上の危険を生じるおそれがある物であってはならない。」と定められています。つまり、安全であることが全ての化粧品原料の絶対条件です。
- ネガティブリスト:原則使用禁止の成分/ 化粧品基準の「2 防腐剤、紫外線吸収剤及びタール色素以外の成分の配合の禁止」と「3 防腐剤、紫外線吸収剤及びタール色素以外の成分の配合の制限」の項目は、通称「ネガティブリスト」と呼ばれます。ここには、医薬品成分など、化粧品への配合が一切禁止されている成分や、配合量に上限が定められている成分がリストアップされています。処方開発の際は、これらの成分を意図せず配合してしまわないよう、細心の注意が必要です。
- ポジティブリスト:特定の目的でのみ使用が許可される成分/ 化粧品基準の「4 防腐剤、紫外線吸収剤及びタール色素」の項目は、通称「ポジティブリスト」と呼ばれます。防腐剤、紫外線吸収剤、タール色素については、このリストに収載されている成分でなければ使用することができず、さらに各成分には配合量の上限が定められています。ただし、赤色219号及び黄色204号については、毛髪及び爪のみに使用される化粧品に限り配合することができると化粧品基準で定められています。。
- グリセリンの成分規制/ 化粧品基準の「5」ではグリセリンに関する規定(ジエチレングリコール 0.1%以下のグリセリンしか使用不可の旨)があります。これは平成20年2月に追加されました。
化粧品基準をクリアしていることの確認方法
この化粧品基準による成分規制をクリアしているか否かの確認ですが、「購入した原料や化粧品を何らかの科学的検査にかけて、◯◯という成分が◯%、△△という成分が△%…というような結果がえられる」というような魔法の方法は残念ながらありません。
原料の場合には、信頼できる原料メーカーから提供される成分情報(試験成績書など)を基に、化粧品基準をクリアできるように処方を組むという作業が基本かと思います。この原料に対しては得た資料と齟齬がないかの確認検査を行うことも多々です。
化粧品現物の場合には、ポジティブリスト、ネガティブリストなどの逸脱リスクの高い成分についてピーク値を確認するといった「成分分析」はよく行われているところでしょう。特に海外からの輸入化粧品に対してはよくやりますね。
どういった方法を取るにせよ、「検査にかけることはコスト、でも逸脱リスクを背負うのは製造販売業者」ですから、情報の信頼性や配合成分から推察されるリスクの高さなどから、適切な検査を設定するのが品質管理の腕の見せ所だと思います。
③生物由来原料基準(平成15年厚生労働省告示第210号)

動物やヒトなどの生物に由来する原料(プラセンタ、コラーゲン、スクワランなど)を使用する場合に適用される基準です。これも化粧品基準と同じく薬機法第42条第2項を根拠としています。
薬機法第56条第5号から生物由来原料基準を導く
化粧品基準のところに書いたのと同じです。
生物由来原料基準の内容
生物由来原料基準(平成15年厚生労働省告示第210号)(PMDAが公開している生物由来原料基準へのリンク)は、以下の要素で構成されています。
- 第1 通則
- 第2 血液製剤総則
- 1 輸血用血液製剤総則
- 2 血漿分画製剤総則
- 第3 人由来製品原料総則
- 1 人細胞組織製品原料基準
- 2 人尿由来原料基準
- 3 人由来原料基準
- 第4 動物由来製品原料総則
- 1 反芻動物由来原料基準
- 2 動物細胞組織製品原料基準
- 3 動物由来原料基準
生物由来原料基準をクリアしていることの確認方法
メーカーにヒアリングするしかありません。原産地証明や製造工程図により文書により明示してもらうのが一番です。
特に輸入実務において最も神経を使うのがBSE(牛海綿状脳症)対策です。牛、羊、山羊などの反芻動物に由来する成分が含まれる場合、以下の詳細な情報の精査が求められます。
- 原産国: BSE発生国ではないか。
- 部位: 脳、脊髄、眼、回腸遠位部などの「特定部位」が含まれていないか。
- 処理工程: 病原体を不活化させるための適切な処理がなされているか。
- 実務上の注意点: 海外メーカーは「安全だ」と一言で済ませがちですが、日本の基準では「Certificate of Origin(原産地証明)」や「Manufacturing Process(製造工程図)」による客観的な証明が必須です。
また近年では、ヒト由来原料を謳った化粧品も多々目にしますので、製造販売業者さんはきちんと確認を取ることが必要です。
④医薬品等に使用することができるタール色素を定める省令(昭和41年厚生省令第30号)
これは薬機法第56条第9号(第62条準用)に基づく制限で、化粧品に使用できる「タール色素」を指定しています。
化粧品基準の内容
医薬品等に使用することができるタール色素を定める省令(昭和41年厚生省令第30号)(厚労省が公開しているタール色素省令へのリンク)は、以下の要素で構成されています。
タール色素省令をクリアしていることの確認方法
じつはこの基準は化粧品基準でも準用されているので、化粧品基準クリアならこの基準もクリアです。
⑤その他自主基準
上述の基準に加え、日本の事業者団体である日本化粧品工業会の自主基準も存在します。
- 揮発性シリコーンの頭髪用化粧品への配合自粛及び注意表示
- デカメチルシクロペンタシロキサン【表示名称: シクロペンタシロキサン】等
- タール色素(法定色素)の使用自粛
- 緑色 205 号、赤色 214 号、赤色 229 号、赤色 502 号、赤色 503 号、赤色 505 号、赤色 506 号、 だいだい色 202 号の (1)、だいだい色 202 号の (2)、だいだい色 402 号、黄色 202 号の(2)、 黄色 403 号の (2)、黄色 404 号、黄色 405 号、黄色 407 号、緑色 402 号
- 赤色 501 号、だいだい色 204 号、だいだい色 403 号
- 赤色 205 号、赤色 206 号、赤色 207 号、赤色 208 号、赤色 404 号
2. 各種試験検査について
微生物に関する試験
薬機法第56条第8号を根拠とする「病原微生物その他疾病の原因となるものにより汚染され、又は汚染されているおそれがないこと」の担保の方法として、法に定められた検査結果は有りません。しかし、一般的には、適切な防腐剤等を配合するなどし保存効力試験をクリアできることが確認された処方で生産工程に移行し、各バルク製造ごとに微生物限度試験を行いってクリアが確認され次第充填等工程に移行します。
業界団体である日本化粧品工業会は、国際規格(ISO 17516)に準拠した自主基準を定めています。
- 保存効力試験(チャレンジテスト)/ 製品に配合されている防腐剤が、有効に機能しているかを確認する試験です。使用中に微生物の混入があっても品質を維持できるか(防腐剤が有効に機能するか)を確認するもので、製品にあえて一定量の微生物を添加し、その後の菌数の推移を観察することで、製品自身の防腐能力を評価します。
- 微生物限度試験/ 製造・出荷時の製品が、微生物に汚染されていないかを確認する試験です。製品中の一般生菌数を測定し、基準値以下であることを確かめます。特に、目の周りに使う製品や乳幼児向け製品は、より厳しい基準値が設定されています。また、大腸菌や黄色ブドウ球菌といった特定の病原菌が検出されないことも確認します。
紫外線防止効果SPFに関する試験
業界団体である日本化粧品工業会は、国際規格(ISO 24444)に準拠した自主基準を定めています。
紫外線防止効果UVAに関する試験
業界団体である日本化粧品工業会は、国際規格(ISO 24442)に準拠した自主基準を定めています。
紫外線防止効果に対する耐水性に関する試験
業界団体である日本化粧品工業会は、国際規格(ISO 18861)に準拠した自主基準を定めています。
3. 安全性試験:人に対する安全性を確認する
処方がほぼ固まってきたら、通常は社内の複数人が実際の使用方法で一定期間使って、使用感や肌状態などを確認します。
これに加えて、必要に応じて、人の肌を使った以下のような専門的な試験を行う場合もあります。
- パッチテスト/ 化粧品を皮膚に貼り付け、皮膚への刺激性を評価する試験です。
- アレルギーテスト(RIPT)/ パッチテストを繰り返し行い、アレルギー反応を誘発する可能性を評価する、より詳細な試験です。
- スティンギングテスト/ 敏感肌の被験者を対象に、使用直後のかゆみ、ヒリヒリといった一過性の刺激を評価する試験です。
ここで挙げたものは代表的な例であり、製品の特性に応じて、これ以外にも様々な人に対する試験が行われることがあります。
4. 安定性試験:品質の「時をかける」保証
製造したての品質が、お客様の手元に届き、使い終わるまで維持されることを保証するのが安定性試験です。これは、GQP省令で求められる品質保証の一環として、極めて重要な試験です。
- 目的: 輸送や保管中に想定される様々な環境(温度、湿度、光など)に製品をさらし、経時的な変化を観察することで、製品の品質が維持される期間、すなわち「有効期間」や「使用期限」を設定することが主な目的です。
- 評価項目: 色、香り、粘度、pHといった物理化学的な性質の変化や、微生物の増殖の有無、容器との適合性などを評価します。
- 試験条件: 加速試験、苛酷試験、長期保存試験などを組み合わせて、多角的に品質の安定性を評価します。
5. 試験はどこで行う?(自社試験と外部委託)
これらの専門的な試験をどこで実施するかは、企業の体制によって異なります。
- 製造業者の自社試験/ ほとんどの化粧品製造業者は、自社内に試験設備を持ち、日常的な品質管理(原料や製品の規格試験など)や、基本的な安定性試験を行っています。
- 外部試験検査機関への委託/ 一方で、パッチテストなどの人に対する安全性試験や、高度な機器を必要とする特殊な分析、あるいはより客観的なデータが求められる場合には、外部の専門的な試験検査機関が活用されます。また、自社で試験設備を持たない製造販売業の許可しか持たない事業者の場合は、これらの試験を外部機関に委託することが一般的です。外部機関を選ぶ際は、GLP(優良試験所規範)等の基準への準拠、化粧品分野での実績、報告書の質などを考慮して、信頼できるパートナーを選定することが重要です。
まとめ:科学的根拠が、ブランドの信頼を創る
化粧品開発における成分確認と各種試験は、単なるコストや手間ではありません。それは、製品の安全性と品質を科学的に保証し、お客様の信頼を獲得するための、最も重要な「投資」です。
薬機法をはじめとする法規制を遵守することはもちろん、これらの試験を適切に実施し、そのデータを客観的な根拠として示すこと。その誠実で科学的な姿勢こそが、お客様に「このブランドなら安心して使える」と感じていただき、長期的に愛される製品とブランドを築き上げていくための、揺ぎない土台となるのです。

こちらの関連記事では、海外からの輸入化粧品の成分確認や新規原料について言及してます。あわせてご確認ください。
GQP、GVPについてはこちらの記事に説明しています。
お気軽にご相談ください。
- 初回相談は無料です。
- 行政書士には秘密保持の義務が課せられております。
- フォームに入力されたメールアドレス以外に、当事務所から連絡差し上げることはいたしません。